题目内容
12.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等(1)下列能说明碳、硫两种元素非金属性相对强弱的是③(填序号)
①沸点:H2S>CH4
②酸性:H2SO3>H2CO3
③CS2中碳元素为+4价,硫元素为-2价
(2)羰基硫(COS)可作为一种熏蒸剂,其分子结构和CO2相似.羰基硫(COS)的电子式为
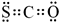 .
.
分析 (1)①沸点的高低与非金属性强弱无关;
②非金属强弱与最高价氧化物对应水化物的酸性强弱有关;
③CS2中碳元素为+4价,硫元素为-2价,说明硫元素对共用电子对的吸引力较强,说明非金属性:S>C;
(2)根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式.
解答 解:(1)①沸点的高低与非金属性强弱无关,故不选;
②非金属强弱与最高价氧化物对应水化物的酸性强弱有关,故不选;
③CS2中碳元素为+4价,硫元素为-2价,说明硫元素对共用电子对的吸引力较强,说明非金属性:S>C,故选;故答案为:③;
(2)羰基硫中分子中所有原子的最外层都满足8电子结构,碳原子能形成4个共价键,硫原子能形成2个共价键,氧原子能形成2个共价键,所以其电子式为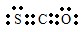 ,
,
故答案为: .
.
点评 本题考查了物质结构元素周期律,综合性较强,掌握同一周期元素性质递变规律,明确元素最高价氧化物的水化物酸碱性是解本题②的关键,题目难度中等.

练习册系列答案
相关题目
19.某有机物2.3克,完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,该有机物的分子式是( )
| A. | C2H6O | B. | C2H4O | C. | C2H6 | D. | C2H4 |
20.短周期主族元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.下列推测不正确的是( )
| A. | 元素Y的最高价氧化物的水化物是强酸 | |
| B. | 三种元素的原子半径:r(X)>r(Z)>r(Y) | |
| C. | Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | 由X与Z两种元素组成的离子化合物不止一种. |
17.某无色透明溶液中加入铝粉,有大量氢气放出,则该溶液可能存在的离子组是( )
| A. | NH4+、Na+、Cl-、I- | B. | K+、NO3-、Mg2+、SO42- | ||
| C. | Na+、Cu2+、Cl-、SO42- | D. | Na+、K+、HCO3-、Cl- |
7.下列反应中,水作氧化剂的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | CuO+H2 $\frac{\underline{\;高温\;}}{\;}$ Cu+H2O | D. | Na2O+H2O═2NaOH |
1.下列说法正确的是( )
| A. | 煤的干馏、石油的分馏分别是化学变化、物理变化 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,二者是同分异构体 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | 饱和(NH4)2SO4溶液和饱和CuSO4溶液都能使蛋白质溶液产生沉淀,其作用原理相同 |
2.烷烃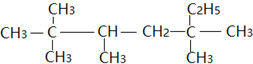 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
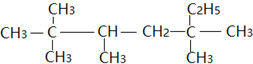 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
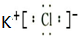 ,B元素基态原子的电子排布图为
,B元素基态原子的电子排布图为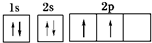 .
.