题目内容
12.当氨完全分解成氮气和氢气时,混合气体对空气的相对密度为( )| A. | 1.17 | B. | 0.74 | C. | 0.293 | D. | 1.03 |
分析 当氨完全分解成氮气和氢气时,2NH3=N2+3H2,设氨气物质的量为2mol,完全分解生成1molN2,3molH2,平均摩尔质量=$\frac{1mol×28g/mol+3mol×2g/mol}{1mol+3mol}$=8.5g/mol,相同条件下气体密度之比等于其相对分子质量之比,密度之比为相对密度.
解答 解:当氨完全分解成氮气和氢气时,2NH3=N2+3H2,设氨气物质的量为2mol,完全分解生成1molN2,3molH2,平均摩尔质量=$\frac{1mol×28g/mol+3mol×2g/mol}{1mol+3mol}$=8.5g/mol,相同条件下气体密度之比等于其相对分子质量之比,空气的平均相对分子质量为29,密度之比为相对密度,则混合气体对空气的相对密度=$\frac{8.5}{29}$=0.293,
故选C.
点评 本题考查了化学方程式、混合气体相对分子质量、相对密度的计算应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
3.有机物A可用于制备常见的解热镇痛药阿司匹林.纯净的A为白色结晶性粉末,易溶于水.为研究A的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| (1)称取A 6.9g,升温使其汽化,测其密度是相同条件下CH4的8.625倍. | (1)A的相对分子质量为:138. |
| (2)将此6.9g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和15.4g | (2)A的分子式为:C7H6O3. |
| (3)另取A 6.9g,跟足量的NaHCO3粉末反应,生成1.12L CO2(标准状况),若与足量金属钠反应则生成1.12L H2(标准状况). | (3)用结构简式表示A中含有的官能团: -OH、-COOH. |
| (4)A的核磁共振氢谱显示A有6种氢 | A的结构简式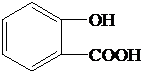 |
(5)写出A与浓溴水反应的方程式: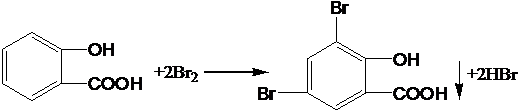 | |
20.短周期主族元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.下列推测不正确的是( )
| A. | 元素Y的最高价氧化物的水化物是强酸 | |
| B. | 三种元素的原子半径:r(X)>r(Z)>r(Y) | |
| C. | Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | 由X与Z两种元素组成的离子化合物不止一种. |
7.28%的KOH溶液中,平均溶有一个OH-所需的水分子的个数为( )
| A. | 6个 | B. | 8个 | C. | 10个 | D. | 28个 |
17.某无色透明溶液中加入铝粉,有大量氢气放出,则该溶液可能存在的离子组是( )
| A. | NH4+、Na+、Cl-、I- | B. | K+、NO3-、Mg2+、SO42- | ||
| C. | Na+、Cu2+、Cl-、SO42- | D. | Na+、K+、HCO3-、Cl- |
7.下列反应中,水作氧化剂的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | CuO+H2 $\frac{\underline{\;高温\;}}{\;}$ Cu+H2O | D. | Na2O+H2O═2NaOH |
5.下列反应中不是氧化还原反应的是( )
| A. | 3Cl2+6KOH═5KCl+KClO3+3H2O | B. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2AgNO3+BaCl2═2AgCl↓+Ba(NO3)2 |

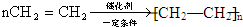 .
.