题目内容
5.等温、等压下,Ag CO2所占的体积为11.2L,0.5A g X的气体所占的体积为7.7L,则气体的相对分子质量为( )| A. | 16 | B. | 32 | C. | 48 | D. | 64 |
分析 根据PV=nRT=$\frac{m}{M}$RT可知,$\frac{11.2×44}{7.7×{M}_{X}}=\frac{A}{0.5A}$,由此解答.
解答 解:根据PV=nRT=$\frac{m}{M}$RT可知,$\frac{11.2×44}{7.7×{M}_{X}}=\frac{A}{0.5A}$,解之得:MX=32,故选:B.
点评 本题考查阿伏伽德罗定律及其推论,明确体积、质量和摩尔质量之间的关系是解本题的关键,难度不大.

练习册系列答案
相关题目
15.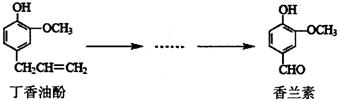 香兰素是重要的香料之一,它可由丁香油酚多步反应合成.有关上述两种化合物的说法正确的是( )
香兰素是重要的香料之一,它可由丁香油酚多步反应合成.有关上述两种化合物的说法正确的是( )
 香兰素是重要的香料之一,它可由丁香油酚多步反应合成.有关上述两种化合物的说法正确的是( )
香兰素是重要的香料之一,它可由丁香油酚多步反应合成.有关上述两种化合物的说法正确的是( )| A. | 在丁香油酚分子中至少有12个原子共平面 | |
| B. | 常温下,1mol丁香油酚可与2molBr2反应 | |
| C. | 1moI香兰素最多能与4mol氢气发生加成反应 | |
| D. | 可用酸性KMnO4溶液检验丁香油酚中是否含有碳碳双键 |
16.四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
| A. | W与X形成的化合物溶于水后溶液呈碱性 | |
| B. | 简单离子半径:W<X<Z | |
| C. | 气态氢化物的热稳定性:W<Y | |
| D. | 最高价氧化物的水化物的酸性:Y>Z |
13.已知短周期元素的离子:aAm+、bBn+、cCm-、dDn-(m>n)都具有相同的电子层结构,则下列叙述正确的是( )
①原子半径:A>B>C>D
②离子半径:C>D>B>A
③原子序数:d>c>b>a
④最外层电子数:D>C>B>A
⑤金属性:B>A>D>C
⑥a-b=m+n
⑦b-c=m+n.
①原子半径:A>B>C>D
②离子半径:C>D>B>A
③原子序数:d>c>b>a
④最外层电子数:D>C>B>A
⑤金属性:B>A>D>C
⑥a-b=m+n
⑦b-c=m+n.
| A. | ②④⑦ | B. | ②⑤⑥ | C. | ①⑤⑦ | D. | ②⑦ |
20.短周期主族元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期.下列推测不正确的是( )
| A. | 元素Y的最高价氧化物的水化物是强酸 | |
| B. | 三种元素的原子半径:r(X)>r(Z)>r(Y) | |
| C. | Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | 由X与Z两种元素组成的离子化合物不止一种. |
10.在元素R的原子中,最外层上的电子数比次外层上的电子数多2个,则R不能形成的化台物是( )
| A. | RO | B. | R2H4 | C. | HRO2 | D. | H2R2O4 |
17.某无色透明溶液中加入铝粉,有大量氢气放出,则该溶液可能存在的离子组是( )
| A. | NH4+、Na+、Cl-、I- | B. | K+、NO3-、Mg2+、SO42- | ||
| C. | Na+、Cu2+、Cl-、SO42- | D. | Na+、K+、HCO3-、Cl- |
18.下列各组元素性质递变情况错误的是( )
| A. | P、S、Cl最高正价依次升高 | |
| B. | Li、Be、B原子最外层电子数逐渐增多 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
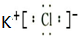 ,B元素基态原子的电子排布图为
,B元素基态原子的电子排布图为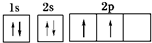 .
.