��Ŀ����
 �ס���̽��С��ͬѧ�������仯��������ʽ�����̽�����Իش��������⣺
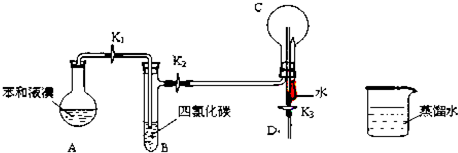
�ס���̽��С��ͬѧ�������仯��������ʽ�����̽�����Իش��������⣺��1������ͬѧ������ͼװ��̽������ŨH2SO4�ķ�Ӧ��������������һ������Ũ�������ʱ��Ӧ�Ļ�ѧ����ʽΪ
�ټ����װ�õ������Եķ�����
������ɷ���
��ȡ������Ӧ�����Һ���ȵμ�����������ˮ���ٵμ�KSCN��Һ������Ѫ��ɫ�������μӹ���������ˮ����ɫ��ȥ����������ܵ�ԭ���ǣ�
A����Һ��Fe3+�������̸���̬������
B��
C��
���ú��ʵĻ�ѧ�Լ�����֤����A�Ƿ���ȷ��
��ѡ���Լ��У�0.1mol/L FeCl3��Һ��1mol/L FeCl2��Һ��1mol/L KSCN��Һ��������ˮ��һ��Ũ�ȵ�H2O2��Һ������Ϊ
��2������ͬѧ������������������ϡ���ᷴӦ��ʵ�飮ȡmgFe��FeO��ɵĻ�����뺬2molHNO3���ʵ�ϡ�����ַ�Ӧ����HNO3ֻ����ԭ��NO���ҷ�Ӧ��������Һ����ȫ��Fe3+���������������m��ȡֵ��Χ��
���㣺����ʵ�鷽�������,̽�����ʵ���ɻ�������ʵĺ���
ר�⣺ʵ�������
��������1��Ũ������������ڼ��������·�Ӧ�������������Ͷ����������壬���ŷ�Ӧ�Ľ��У������Ũ�����ͣ�ϡ���������Ӧ�������������ü��ȵķ����γ�ѹǿ�������������ԣ�ȡ������Ӧ�����Һ���ȵμ�����������ˮ���ٵμ�KSCN��Һ������Ѫ��ɫ�������μӹ���������ˮ����ɫ��ȥ�����ܴ��ڵ��������Һ��Fe3+�������̸���̬��������Һ��SCN-����������Һ��Fe3+��SCN-���������������Լ��ķ��μӷ����飻
��2�����跴Ӧ��ΪFe��FeO������������ö�ֵ�����㣮
��2�����跴Ӧ��ΪFe��FeO������������ö�ֵ�����㣮
���
�⣺��1��Ũ������������ڼ��������·�Ӧ�������������Ͷ����������壬��Ӧ�Ļ�ѧ����ʽΪFe+2H2SO4��Ũ��
FeSO4+SO2��+2H2O��
�ʴ�Ϊ��Fe+2H2SO4��Ũ��
FeSO4+SO2��+2H2O��
�ټ�������ԣ�������Ͳ�м���һ�����������ˮ��û������ĩ�ˣ��þƾ�����Բ����ƿ��������ĩ�˳������ݣ���ֹͣ���Ⱥ����г���һ���ȶ���Һ����˵��װ�����������ã�
�ʴ�Ϊ������Ͳ�м���һ�����������ˮ��û������ĩ�ˣ��þƾ�����Բ����ƿ��������ĩ�˳������ݣ���ֹͣ���Ⱥ����г���һ���ȶ���Һ����˵��װ�����������ã�
��Ũ������������ڼ��������·�Ӧ�������������Ͷ����������壬���ŷ�Ӧ�Ľ��У������Ũ�����ͣ�ϡ���������Ӧ����������
�ʴ�Ϊ��SO2��H2��
��ȡ������Ӧ�����Һ���ȵμ�����������ˮ���ٵμ�KSCN��Һ������Ѫ��ɫ�������μӹ���������ˮ����ɫ��ȥ�����ܴ��ڵ��������Һ��Fe3+�������̸���̬��������Һ��SCN-����������Һ��Fe3+��SCN-����������
�������Һ�е�+3����������Ϊ���ߵļ�̬�����ټ�FeCl3��Һ��������ɫ����Һ��ȡ����Һ��������һ�Թ��У��ټ���������1mol/L��FeCl3��Һ�������Һ��ɫ��ԭ�������A��ȷ����֮��Ȼ��
�ʴ�Ϊ����Һ��SCN-����������Һ��Fe3+��SCN-����������������ɫ����Һ��ȡ����Һ��������һ�Թ��У��ټ���������1mol/L��FeCl3��Һ�������Һ��ɫ��ԭ�������A��ȷ����֮��Ȼ��
��2�������ȫ��ΪFe�������ʵ���Ϊxmol��ʧȥ3xmol���ӣ���Ӧ����Fe��NO3��3��NO��������NO�����ʵ���Ϊxmol��Fe��NO3��3�����ʵ���Ϊ3xmol��
����n��N0��+3n��Fe��NO3��3��=4xmol=2mol��
x=0.5��
m��Fe��=0.5mol��56g/mol=28g��
�����ȫ��ΪFeO�������ʵ���Ϊymol��ʧȥymol���ӣ���Ӧ����Fe��NO3��3��NO��������NO�����ʵ���Ϊ
ymol��Fe��NO3��3�����ʵ���Ϊ3ymol��
����n��N0��+3n��Fe��NO3��3��=��3y+
y��mol=2mol��
y=0.6mol��
m��FeO��=0.6mol��72g/mol=43.2g��
�������������m��ȡֵ��Χ�ǣ�
�ʴ�Ϊ��28��m��43.2��
| ||
�ʴ�Ϊ��Fe+2H2SO4��Ũ��
| ||
�ټ�������ԣ�������Ͳ�м���һ�����������ˮ��û������ĩ�ˣ��þƾ�����Բ����ƿ��������ĩ�˳������ݣ���ֹͣ���Ⱥ����г���һ���ȶ���Һ����˵��װ�����������ã�
�ʴ�Ϊ������Ͳ�м���һ�����������ˮ��û������ĩ�ˣ��þƾ�����Բ����ƿ��������ĩ�˳������ݣ���ֹͣ���Ⱥ����г���һ���ȶ���Һ����˵��װ�����������ã�
��Ũ������������ڼ��������·�Ӧ�������������Ͷ����������壬���ŷ�Ӧ�Ľ��У������Ũ�����ͣ�ϡ���������Ӧ����������
�ʴ�Ϊ��SO2��H2��
��ȡ������Ӧ�����Һ���ȵμ�����������ˮ���ٵμ�KSCN��Һ������Ѫ��ɫ�������μӹ���������ˮ����ɫ��ȥ�����ܴ��ڵ��������Һ��Fe3+�������̸���̬��������Һ��SCN-����������Һ��Fe3+��SCN-����������
�������Һ�е�+3����������Ϊ���ߵļ�̬�����ټ�FeCl3��Һ��������ɫ����Һ��ȡ����Һ��������һ�Թ��У��ټ���������1mol/L��FeCl3��Һ�������Һ��ɫ��ԭ�������A��ȷ����֮��Ȼ��
�ʴ�Ϊ����Һ��SCN-����������Һ��Fe3+��SCN-����������������ɫ����Һ��ȡ����Һ��������һ�Թ��У��ټ���������1mol/L��FeCl3��Һ�������Һ��ɫ��ԭ�������A��ȷ����֮��Ȼ��
��2�������ȫ��ΪFe�������ʵ���Ϊxmol��ʧȥ3xmol���ӣ���Ӧ����Fe��NO3��3��NO��������NO�����ʵ���Ϊxmol��Fe��NO3��3�����ʵ���Ϊ3xmol��
����n��N0��+3n��Fe��NO3��3��=4xmol=2mol��
x=0.5��
m��Fe��=0.5mol��56g/mol=28g��
�����ȫ��ΪFeO�������ʵ���Ϊymol��ʧȥymol���ӣ���Ӧ����Fe��NO3��3��NO��������NO�����ʵ���Ϊ
| 1 |
| 3 |
����n��N0��+3n��Fe��NO3��3��=��3y+
| 1 |
| 3 |
y=0.6mol��
m��FeO��=0.6mol��72g/mol=43.2g��
�������������m��ȡֵ��Χ�ǣ�
�ʴ�Ϊ��28��m��43.2��
���������⿼�����ʵ�����ʵ��̽���ͻ����ļ��㣬Ϊ�߿��������ͣ�������ѧ���ķ�����ʵ��ͼ��������Ŀ��飬ע�����ʵ��ķ����Ͷ�ֵ���ļ����˼·���Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
��NA��ʾ�����ӵ�������ֵ������˵������ȷ���ǣ�������
| A�����³�ѹ�£�3.0 g�����к��е�̼�����Ϊ0.7NA |
| B����0.2 mol FeCl3ˮ���Ƴɽ��壬���ý���������Ϊ 0.2NA |
| C�����³�ѹ�£�28 g�� C2H4��C3H6������庬�е�ԭ����Ϊ 6NA |
| D����״���£���Na2O2�Ƶ�11.2 L O2����Ӧת�Ƶĵ�����Ϊ0.5NA |
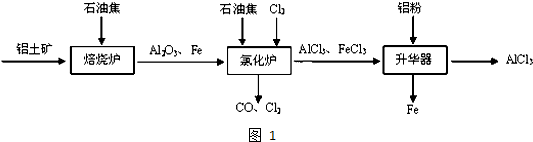
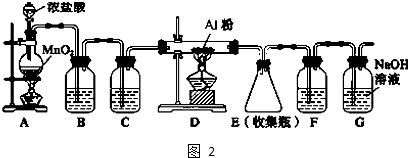
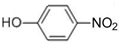 ��
��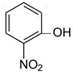 ��I2 ��H2O2 ��SiO2 ��NH4Cl
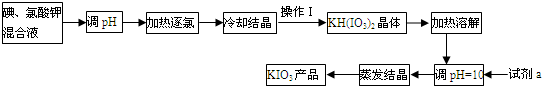
��I2 ��H2O2 ��SiO2 ��NH4Cl �������Ʊ�����Ѫҩ��ͨ����ͼ·�ߺϳɣ�
�������Ʊ�����Ѫҩ��ͨ����ͼ·�ߺϳɣ�