题目内容
无水AlCl3可用作有机合成的催化剂,食品膨松剂等.已知AlCl3、FeCl3分别在183℃、315℃时升华,无水AlCl3遇潮湿空气即产生大量白雾.
Ⅰ.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如图1:
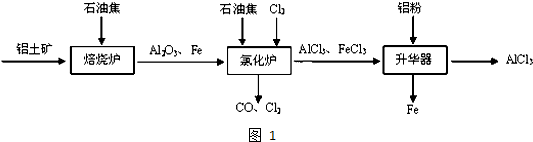
(1)焙烧炉中发生反应:①Fe2O3(s)+3C(s)?2Fe(s)+3CO(g);
②3CO(g)+Fe2O3(s)?2Fe(s)+3CO2(g)
则反应②的平衡常数的表达式为K= .
(2)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为 ;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为 .
(3)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%.现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g.该样品中AlCl3的质量分数为 .
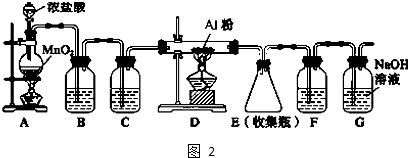
Ⅱ.实验室可用如图2装置制备无水AlCl3.装置B、C中应盛放的试剂名称分别为 、 ,F中所盛放试剂的作用是 .
Ⅰ.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如图1:

(1)焙烧炉中发生反应:①Fe2O3(s)+3C(s)?2Fe(s)+3CO(g);
②3CO(g)+Fe2O3(s)?2Fe(s)+3CO2(g)
则反应②的平衡常数的表达式为K=
(2)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为
(3)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%.现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g.该样品中AlCl3的质量分数为
Ⅱ.实验室可用如图2装置制备无水AlCl3.装置B、C中应盛放的试剂名称分别为

考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题,化学实验与化学计算
分析:Ⅰ、铝土矿加入碳焙烧后加入氧化铝和铁于氯化炉中发生反应氧化铝解饿碳和氯气加热反应生成氯化铝和一氧化碳,AlCl3、FeCl3分别在183℃、315℃时升华,控制温度升华氯化铝得到;
(1)依据反应②化学方程式书写表达式,用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
(2)根据工艺流程可知升华器中含有AlCl3等,所以Al2O3、C12和C反应会生成A1C13,由冷凝器尾气可知还会生成CO;Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-;
(3)制备无水AlCl3含有杂质FeCl3,残留固体质量为0.32g为Fe2O3,根据铁原子守恒计算FeCl3质量,进而计算出AlCl3的质量,再根据产品的纯度定义计算.
Ⅱ、根据所给的装置图可知,B中的试剂为饱和食盐水是为了除去混有的HCl气体,C中是浓硫酸目的是除去水蒸气;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶.
(1)依据反应②化学方程式书写表达式,用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
(2)根据工艺流程可知升华器中含有AlCl3等,所以Al2O3、C12和C反应会生成A1C13,由冷凝器尾气可知还会生成CO;Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-;
(3)制备无水AlCl3含有杂质FeCl3,残留固体质量为0.32g为Fe2O3,根据铁原子守恒计算FeCl3质量,进而计算出AlCl3的质量,再根据产品的纯度定义计算.
Ⅱ、根据所给的装置图可知,B中的试剂为饱和食盐水是为了除去混有的HCl气体,C中是浓硫酸目的是除去水蒸气;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶.
解答:
解:Ⅰ、(1)②3CO(g)+Fe2O3(s)?2Fe(s)+3CO2(g),反应②的平衡常数的表达式为K=
;
故答案为:
;
(2)根据工艺流程可知氯化炉的产物,经冷却、升华可制备无水AlCl3,说明氯化炉的产物中含有A1C13,冷凝器尾气含有CO,所以Al2O3、C12和C反应,生成A1C13和CO,反应方程式为A12O3+3C12+3C
2A1C13+3CO,Cl2有强氧化性,将SO32-氧化为SO42-,自身被还原为2C1-.反应离子方程式为SO32-+C12+H2O═SO42-+2C1-+2H+,
故答案为:A12O3+3C12+3C
2A1C13+3CO;SO32-+C12+H2O═SO42-+2C1-+2H+;
(3)除杂过程中铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水,离子方程式为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O,根据铁原子守恒,令含有杂质FeCl3质量为m,则:
Fe2O3~~~~~2FeCl3
160 325
0.16g m
解得,m=0.325g,
所以AlCl3产品的纯度为
×100%=98%,
故答案为:98%;
Ⅱ、根据所给的装置图可知,B中的试剂为饱和食盐水是为了除去混有的HCl气体,C中是浓硫酸目的是除去水蒸气;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶;
故答案为:饱和食盐水,浓硫酸,防止水蒸气进入E装置;
| c3(CO2) |
| c3(CO) |
故答案为:
| c3(CO2) |
| c3(CO) |
(2)根据工艺流程可知氯化炉的产物,经冷却、升华可制备无水AlCl3,说明氯化炉的产物中含有A1C13,冷凝器尾气含有CO,所以Al2O3、C12和C反应,生成A1C13和CO,反应方程式为A12O3+3C12+3C
| ||
故答案为:A12O3+3C12+3C
| ||
(3)除杂过程中铁离子与氢氧根离子结合成氢氧化铁沉淀,铝离子与氢氧根离子结合成偏铝酸根和水,离子方程式为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O,根据铁原子守恒,令含有杂质FeCl3质量为m,则:
Fe2O3~~~~~2FeCl3
160 325
0.16g m
解得,m=0.325g,
所以AlCl3产品的纯度为
| 16.25g-0.325g |
| 16.25g |
故答案为:98%;
Ⅱ、根据所给的装置图可知,B中的试剂为饱和食盐水是为了除去混有的HCl气体,C中是浓硫酸目的是除去水蒸气;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶;
故答案为:饱和食盐水,浓硫酸,防止水蒸气进入E装置;
点评:本题考查学生对于工艺流程原理的理解、对操作与实验条件控制的理解等,涉及常用化学用语书写、化学计算、分离提纯等,需要学生具备扎实的基础与综合运用能力,难度中等.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
下列叙述正确的是( )
| A、CO2的摩尔质量为44g |
| B、5.4gH2O中有1.806×1023个原子 |
| C、CH4的相对分子质量为16g |
| D、2mol Cl2和2mol CO2所含分子数相等 |
下列四种基本类型的反应中,一定不是氧化还原反应的是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
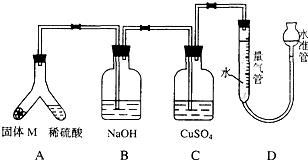 某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)
某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)


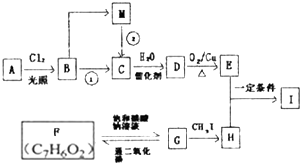
 甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题:
甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题: