题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,3.0 g乙烷中含有的碳氢键数为0.7NA |
| B、将0.2 mol FeCl3水解制成胶体,所得胶体粒子数为 0.2NA |
| C、常温常压下,28 g的 C2H4和C3H6混合气体含有的原子数为 6NA |
| D、标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.乙烷分子中含有6个碳氢键,乙烷的摩尔质量为30g/mol;
B.氢氧化铁胶体粒子是氢氧化铁的聚集体,无法计算生成胶粒的数目;
C.根据二者的最简式进行计算含有的原子数目;
D.标况下11.2L氧气的物质的量为0.5mol,由过氧化钠制取0.5mol氧气需要转移1mol电子.
B.氢氧化铁胶体粒子是氢氧化铁的聚集体,无法计算生成胶粒的数目;
C.根据二者的最简式进行计算含有的原子数目;
D.标况下11.2L氧气的物质的量为0.5mol,由过氧化钠制取0.5mol氧气需要转移1mol电子.
解答:
解:A.3.0g乙烷的物质的量为0.1mol,0.1mol乙烷分子中含有0.6mol碳氢键,含有的碳氢键数为0.6NA,故A错误;
B.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算氢氧化铁胶粒的物质的量及数目,故B错误;
C.常温常压下,28g的C3H6和C4H8混合气体中含有2mol最简式CH2,含有6mol原子,食盐含有的原子数为6NA,故C正确;
D.用过氧化钠制取标况下11.2L氧气,氧气的物质的量为0.5mol,转移的电子为1mol,转移的电子数为NA,故D错误.
故选C.
B.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算氢氧化铁胶粒的物质的量及数目,故B错误;
C.常温常压下,28g的C3H6和C4H8混合气体中含有2mol最简式CH2,含有6mol原子,食盐含有的原子数为6NA,故C正确;
D.用过氧化钠制取标况下11.2L氧气,氧气的物质的量为0.5mol,转移的电子为1mol,转移的电子数为NA,故D错误.
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意过氧化钠中的氧元素化合价为-1价.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学基本用语或表达正确的是( )
| A、Cu原子的激发态简化电子排布式为[Ar]3d104s1 |
| B、Fe原子的外围电子排布式为4s2 |
C、丙烷分子的比例模型: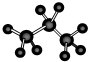 |
D、CH4Si的结构式: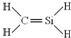 |
下列叙述正确的是( )
| A、CO2的摩尔质量为44g |
| B、5.4gH2O中有1.806×1023个原子 |
| C、CH4的相对分子质量为16g |
| D、2mol Cl2和2mol CO2所含分子数相等 |
同温同压下,等质量的下列各组气体含有相同数目的原子数的是( )
| A、O2与O3 |
| B、SO2与SO3 |
| C、CO2与CO |
| D、CO与N2 |
标准状况下有①6.72L甲烷 ②3.01×1023个氯化氢分子 ③13.6g硫化氢④0.2mol NH3.下列对这四种气体的关系从小到大表示不正确的是( )
| A、体积:④<①<②<③ |
| B、密度:①<④<③<② |
| C、质量:④<①<③<② |
| D、氢原子数:②<④<③<① |
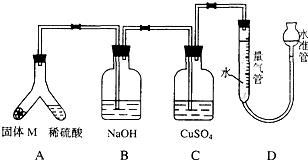 某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)
某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如图装置.倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化,反应后进入量气管气体的体积为VmL(已折算成标准状况)


 甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题:
甲、乙探究小组同学对铁及其化合物的性质进行了探究,试回答下列问题: