��Ŀ����
�ӵ�ʳ������������صĹ�ҵ����������ͼ��
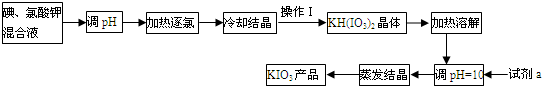
��1����֪��Ӧ�������ķ�Ӧ�У����ֻ�ԭ�������õ�������ͬ������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��
I2+ KClO3+ H2O�T KH��IO3��2+ KCl+ Cl2��
��2��������������������� ���գ����ӷ���ʽΪ ��
��3�������������Ϊ ���Լ�aΪ �������Լ�a������Ӧ�Ļ�ѧ����ʽΪ
��
��4������KIO3��Ʒ��KIO3�ĺ������õ������ⶨ��ȷ����KIO3��Ʒ0.2500g�����������KI��Һ��������ϡ�����ữ������I2���ټ���2��3�ε�����Һ����0.3000mol/LNa2S2O3����Һ�ζ�I2�����ﵽ�ζ��յ�ʱ������Na2S2O3��Һ20.00mL�������ķ�Ӧ���£�IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
����ʵ��ﵽ�ζ��յ�������� ����KIO3��Ʒ��KIO3����������Ϊ ��

��1����֪��Ӧ�������ķ�Ӧ�У����ֻ�ԭ�������õ�������ͬ������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��
��2���������������������
��3�������������Ϊ
��4������KIO3��Ʒ��KIO3�ĺ������õ������ⶨ��ȷ����KIO3��Ʒ0.2500g�����������KI��Һ��������ϡ�����ữ������I2���ټ���2��3�ε�����Һ����0.3000mol/LNa2S2O3����Һ�ζ�I2�����ﵽ�ζ��յ�ʱ������Na2S2O3��Һ20.00mL�������ķ�Ӧ���£�IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
����ʵ��ﵽ�ζ��յ��������
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��
ר�⣺ʵ�������
�������������ػ����Һ������ҺPH���ȸϳ�������ȴ�ᾧͨ�����˵õ�KH��IO3��2 ���壬�����ܽ⣬��������������Һ������ҺPH=10�õ���Һ����Ũ����ȴ�ᾧ�õ�����ؾ��壻
��1������������ԭ��Ӧ�����غ㣬ԭ���غ���ƽ��д���ӷ���ʽ����Ԫ�ػ��ϼ�0�۱仯Ϊ+5�ۣ���Ԫ�ػ��ϼ�+5�۱仯Ϊ0�ۺ�-1�ۣ�
��2����������������������Һ���գ�
��3���������Ƿ���������Һ�����ù��˷��룬�Լ�a�ǵ�����ҺPH=10�������Լ����������µ����ʣ�KH��IO3��2��KOH��Ӧ����2KIO3��H2O��
��4���ζ��յ������õ��������ⵥ�ʱ���ɫ���淴Ӧ������ɫ��ȥ���Ұ�����ڲ����ָ���ɫ����Ϸ�Ӧ������ϵ�����ӷ���ʽ������Ʒ�е��������������
��1������������ԭ��Ӧ�����غ㣬ԭ���غ���ƽ��д���ӷ���ʽ����Ԫ�ػ��ϼ�0�۱仯Ϊ+5�ۣ���Ԫ�ػ��ϼ�+5�۱仯Ϊ0�ۺ�-1�ۣ�
��2����������������������Һ���գ�
��3���������Ƿ���������Һ�����ù��˷��룬�Լ�a�ǵ�����ҺPH=10�������Լ����������µ����ʣ�KH��IO3��2��KOH��Ӧ����2KIO3��H2O��
��4���ζ��յ������õ��������ⵥ�ʱ���ɫ���淴Ӧ������ɫ��ȥ���Ұ�����ڲ����ָ���ɫ����Ϸ�Ӧ������ϵ�����ӷ���ʽ������Ʒ�е��������������
���
�⣺��1������������ԭ��Ӧ�����غ㡢ԭ���غ���ƽ��д���ӷ���ʽ Ϊ��6I2+11KClO3+3H2O�T6KH��IO3��2+5KCl+3Cl2����
�ʴ�Ϊ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
��2�������ж������ŷſ����У�����������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ������������Һ��Cl2+2OH-�TCl-+ClO-+H2O��
��3���������Ƿ���������Һ�����ù��˷��룬�Լ�a�ǵ�����ҺPH=10�������Լ����������µ����ʣ����Լ�������������Һ������ҺPH=10��KH��IO3��2��KOH��Ӧ����KIO3��H2O����Ӧ�Ļ�ѧ����ʽΪ��KH��IO3��2+KOH�T2KIO3+H2O��
�ʴ�Ϊ�����ˣ�KOH��Һ��KH��IO3��2+KOH�T2KIO3+H2O��
��4������KIO3��Ʒ��KIO3�ĺ������õ������ⶨ�����������KI��Һ��������ϡ�����ữ������I2���ټ���2��3�ε�����Һ����0.3000mol/LNa2S2O3����Һ�ζ�I2�����ﵽ�ζ��յ�ʱ������Na2S2O3��Һ20.00mL�������ķ�Ӧ���£�IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
����ʵ��ﵽ�ζ��յ�������ǵ��������һ��Na2S2O3��Һ����ƿ����Һ��ɫͻȻ��ȥ���Ұ�����ڲ��ָ���ɫ��
IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
IO3-��3I2+��6S2O32-��
1 6
n 0.3000mol/L��0.020L
n=0.001mol
ȷ����KIO3��Ʒ0.2500g��KIO3����������=
��100%=85.60%
�ʴ�Ϊ�����������һ��Na2S2O3��Һ����ƿ����Һ��ɫͻȻ��ȥ���Ұ�����ڲ��ָ���ɫ��85.60%��
�ʴ�Ϊ��6I2+11KClO3+3H2O=6KH��IO3��2+5KCl+3Cl2����
��2�������ж������ŷſ����У�����������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ������������Һ��Cl2+2OH-�TCl-+ClO-+H2O��
��3���������Ƿ���������Һ�����ù��˷��룬�Լ�a�ǵ�����ҺPH=10�������Լ����������µ����ʣ����Լ�������������Һ������ҺPH=10��KH��IO3��2��KOH��Ӧ����KIO3��H2O����Ӧ�Ļ�ѧ����ʽΪ��KH��IO3��2+KOH�T2KIO3+H2O��
�ʴ�Ϊ�����ˣ�KOH��Һ��KH��IO3��2+KOH�T2KIO3+H2O��
��4������KIO3��Ʒ��KIO3�ĺ������õ������ⶨ�����������KI��Һ��������ϡ�����ữ������I2���ټ���2��3�ε�����Һ����0.3000mol/LNa2S2O3����Һ�ζ�I2�����ﵽ�ζ��յ�ʱ������Na2S2O3��Һ20.00mL�������ķ�Ӧ���£�IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
����ʵ��ﵽ�ζ��յ�������ǵ��������һ��Na2S2O3��Һ����ƿ����Һ��ɫͻȻ��ȥ���Ұ�����ڲ��ָ���ɫ��
IO3-+I-+6H+�T3I2+3H2O��2S2O32-+I2�T2I-+S4O62-��
IO3-��3I2+��6S2O32-��
1 6
n 0.3000mol/L��0.020L
n=0.001mol
ȷ����KIO3��Ʒ0.2500g��KIO3����������=
| 0.001mol��214g/mol |
| 0.25g |
�ʴ�Ϊ�����������һ��Na2S2O3��Һ����ƿ����Һ��ɫͻȻ��ȥ���Ұ�����ڲ��ָ���ɫ��85.60%��
���������⿼�������ʷ����ᴿ��ʵ�鹤����������Ҫ��������������Ӧ�ã�������ԭ��Ӧ������������ӷ���ʽ��д�����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
�������ֻ������͵ķ�Ӧ�У�һ������������ԭ��Ӧ���ǣ�������
| A�����Ϸ�Ӧ | B���ֽⷴӦ |
| C���û���Ӧ | D�����ֽⷴӦ |
ij��Ԫ�������ʽ��NaHA��Һ����pH��7������Һ�и����ӵ�Ũ�ȹ�ϵ����ȷ���ǣ�������
| A��c��Na+����c��HA-����c��H+����c��A2-����c��H2A�� |
| B��c��Na+��+c��H+��=c��HA-��+2c��A2-��+c��OH-�� |
| C��c��H+��+c��A2-��=c��OH-��+c��H2A�� |
| D��c��Na+��=c��HA-��+c��H2A��+c��A2-�� |



 �ס���̽��С��ͬѧ�������仯��������ʽ�����̽�����Իش��������⣺
�ס���̽��С��ͬѧ�������仯��������ʽ�����̽�����Իش��������⣺ ������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯����
������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯����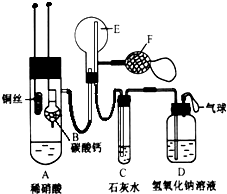 Ϊ��֤��ͭ��ϡ���ᷴӦ��������NO��ijУѧ��ʵ��С�������һ��ʵ�飬��װ����ͼ��ʾ������װ�ú̶�װ�þ�����ȥ����BΪһ���ý���˿�̶��ĸ���ܣ���װ��״̼��ƹ��壻EΪһ���յ�������ƿ��F�����ڹ�������Ĵ�����
Ϊ��֤��ͭ��ϡ���ᷴӦ��������NO��ijУѧ��ʵ��С�������һ��ʵ�飬��װ����ͼ��ʾ������װ�ú̶�װ�þ�����ȥ����BΪһ���ý���˿�̶��ĸ���ܣ���װ��״̼��ƹ��壻EΪһ���յ�������ƿ��F�����ڹ�������Ĵ�����
