题目内容
5.在NaBr和NaI的混合物溶液中通入过量的Cl2把溶液蒸干后并将剩余物灼烧,最后剩余物质是( )| A. | NaCl、Br2、I2 | B. | NaCl | C. | NaCl、Br2 | D. | NaCl、I2 |
分析 向含有NaBr、NaI的溶液中通入过量的Cl2,发生的反应为2NaBr+Cl2=2NaCl+Br2、2NaI+Cl2=I2+2NaCl,溴和碘都不稳定,碘受热易升华,溴易挥发,据此分析解答.
解答 解:向含有NaBr、NaI的溶液中通入过量的Cl2,发生的反应为2NaBr+Cl2=2NaCl+Br2、2NaI+Cl2=I2+2NaCl,溴和碘都不稳定,碘受热易升华,溴易挥发,NaCl属于离子化合物,熔点较高,所以灼烧后最终得到的固体是NaCl,故选B.
点评 本题考查非金属元素之间的置换反应,明确物质的氧化性、物质的物理性质即可解答,熟练掌握同一主族、同一周期元素性质递变规律,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.某溶液可能含有K+、Na+、SO42-、AlO2-、NO3-、I-、Fe2+、Al3+、SiO32-.现进行如下实验:由此可知原溶液中( )
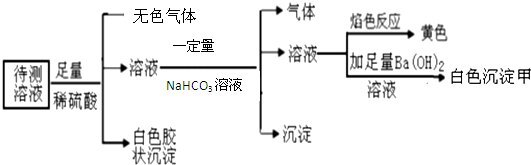

| A. | 一定含有Na+,可能存在K+ | |
| B. | 至少存在4种离子 | |
| C. | 无色气体是NO气体 | |
| D. | 白色沉淀甲中一定含有BaSO4和BaCO3 |
20.将标准状况下2.24L CO2缓慢通入100mL1.5mol•L-1NaOH溶液中(溶液体积变化忽略不计),充分反应后,下列关系正确的是( )
| A. | c(Na+)>c(CO32-)>c(HCO3-) | |
| B. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| C. | c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | c(HCO3-)+2c(CO32-)+c(H2CO3)=1 mol•L-1 |
14.某元素R的最外层电子数是次外层电子数的2倍,由此可以判断( )
| A. | R一定是第2周期元素 | |
| B. | R一定是VA族元素 | |
| C. | R的气态氢化物一定比同周期其他元素气态氢化物稳定 | |
| D. | R气态氢化物化学式为H2R |
15.如表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(用元素符号或化学式作答)
(1)在这些元素中,化学性质最不活泼的是Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,
(3)形成化合物种类最多的元素是C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O
(5)在这些元素中,最活泼的金属在空气中加热反应的产物溶于水时反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的是Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,
(3)形成化合物种类最多的元素是C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O
(5)在这些元素中,最活泼的金属在空气中加热反应的产物溶于水时反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑.
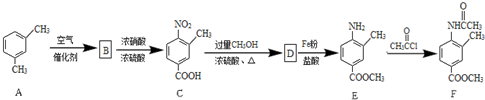
 .
. .
.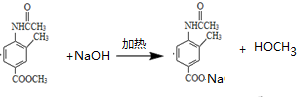 .
.