题目内容
15.如表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的是Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,
(3)形成化合物种类最多的元素是C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O
(5)在这些元素中,最活泼的金属在空气中加热反应的产物溶于水时反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑.
分析 由元素在周期表的位置可知,①为C,②为N,③为O,④为Na,⑤为Al,⑥为S,⑦为Cl,⑧为Ar.
(1)在这些元素中,原子结构中最外层电子数为8的化学性质最不活泼;
(2)在最高价氧化物的水化物中,高氯酸的酸性最强;
(3)有机化合物的种类最多;
(4)N、O、F的氢化物分子间存在氢键;
(5)在这些元素中,最活泼的金属为Na,在空气中加热反应的产物为过氧化钠,溶于水时反应生成NaOH和氧气.
解答 解:由元素在周期表的位置可知,①为C,②为N,③为O,④为Na,⑤为Al,⑥为S,⑦为Cl,⑧为Ar.
(1)在这些元素中,化学性质最不活泼的是Ar,故答案为:Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,故答案为:HClO4;
(3)形成化合物种类最多的元素是C,故答案为:C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O,故答案为:NH3、H2O;
(5)在这些元素中,最活泼的金属为Na,在空气中加热反应的产物为过氧化钠,溶于水时反应生成NaOH和氧气,离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑.
点评 本题考查位置、结构、性质的关系,为高频考点,把握元素的位置、元素周期律、元素化合物的性质为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.在NaBr和NaI的混合物溶液中通入过量的Cl2把溶液蒸干后并将剩余物灼烧,最后剩余物质是( )
| A. | NaCl、Br2、I2 | B. | NaCl | C. | NaCl、Br2 | D. | NaCl、I2 |
10.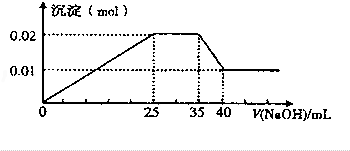 现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )
现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )
 现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )
现有一无色溶液含有以下离子(忽略由水电离产生的H+、OH-):NH4+、Mg2+、Al3+、NO3-,取100mL该溶液并逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如图所示,则NO3-的物质的量是( )| A. | 0.08mol | B. | 0.07mol | C. | 0.06mol | D. | 0.05mol |
20.下列说法不正确的是( )
| A. | 建造三峡大坝使用了大量水泥,水泥属于硅酸盐材料 | |
| B. | 人造刚玉熔点很高,可用作高级耐火材料,主要成分是SiO2 | |
| C. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| D. | 金属冶炼的本质是金属阳离子得到电子变成金属原子 |
7.酸根RO3-所含电子数比硝酸根NO3-的电子数多10,则下列说法正确的是( )
| A. | R和N元素的原子含有相同数目的未成对电子 | |
| B. | RO3-中R的化合价与NO3-中的N的化合价不相等 | |
| C. | RO3-和NO3-只能被还原,不能被氧化 | |
| D. | R原子的电子层数比N的电子层数多1 |
4.下列关于氯水的说法正确的是( )
| A. | 新制氯水中只含氯气和水分子 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 光照氯水有气泡逸出,该气体是氯气 | |
| D. | 氯水放置数天后pH将变大 |
19.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | PCl5 | B. | BF3 | C. | CCl4 | D. | NH3 |
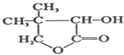 ,G的合成路线如下:
,G的合成路线如下: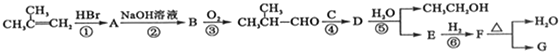
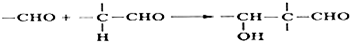
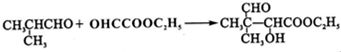 .
.