题目内容
在2L密闭容器中,充入1mol N2和3mol H2,恒温恒容条件下发生合成氨反应,2min时达到平衡.测得平衡时N2的转化率为40%,求:
(1)用H2表示2min内该反应的平均反应速率;
(2)NH3的平衡浓度.
(1)用H2表示2min内该反应的平均反应速率;
(2)NH3的平衡浓度.
考点:化学平衡的计算
专题:化学平衡专题
分析:依据平衡三段式列式计算
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):0.4 1.2 0.8
平衡(mol):0.6 1.8 0.8
(1)用H2表示2min内该反应的平均反应速率=
计算;
(2)NH3的平衡浓度=
计算;
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):0.4 1.2 0.8
平衡(mol):0.6 1.8 0.8
(1)用H2表示2min内该反应的平均反应速率=
| △c |
| △t |
(2)NH3的平衡浓度=
| n |
| V |
解答:
依据平衡三段式列式计算
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):0.4 1.2 0.8
平衡(mol):0.6 1.8 0.8
(1)用H2表示2min内该反应的平均反应速率=
=0.3mol/L?min;
答:用H2表示2min内该反应的平均反应速率为0.3mol/L?min;
(2)NH3的平衡浓度=
=0.4 mol∕L;
答:NH3的平衡浓度为:0.4 mol∕L;
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):0.4 1.2 0.8
平衡(mol):0.6 1.8 0.8
(1)用H2表示2min内该反应的平均反应速率=
| ||
| 2min |
答:用H2表示2min内该反应的平均反应速率为0.3mol/L?min;
(2)NH3的平衡浓度=
| 0.8mol |
| 2L |
答:NH3的平衡浓度为:0.4 mol∕L;
点评:本题考查了化学平衡的计算应用,主要是平衡浓度、反应速率概念的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、H2O和H2O2中的化学键类型完全相同 |
| B、N2的结构式为N-N |
| C、一个H2O分子所含的中子数为8(质量数:H-1,O-16) |
D、NaCl的电子式为 |
下列有关实验原理或操作正确的是( )
A、 稀释浓硫酸 |
B、 闻气体气味 |
C、 称量30.46g的NaOH固体 |
D、 点燃酒精灯 |
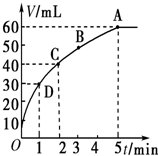 把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.
把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.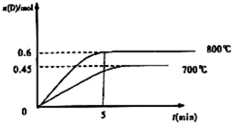 在容积为1L的密闭容器中,进行反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题:
在容积为1L的密闭容器中,进行反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题: