题目内容
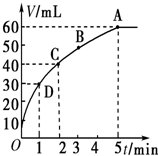 把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.
把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.(1)实验时放出气体的总体积是
(2)放出一半气体所需的时间约为
(3)A、B、C、D各点反应速率快慢的顺序是
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:反应方程式为:2H2O2
2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,根据图象可知生成的氧气的体积,随着反应的进行,溶液的浓度逐渐降低,反应速率逐渐减小.
| ||
解答:
解:(1)由反应方程式为:2H2O2
2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可知,生成氧气的体积为60mL,故答案为:60ml;
(2)由图象可知,当时间进行到1min时,需要的时间为1min,故答案为:1 min;
(3)反应物浓度大小决定反应速率大小,随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小,则V(D)>V(C)>V(B)>V(A),
故答案为:V(D)>V(C)>V(B)>V(A).
| ||
(2)由图象可知,当时间进行到1min时,需要的时间为1min,故答案为:1 min;
(3)反应物浓度大小决定反应速率大小,随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小,则V(D)>V(C)>V(B)>V(A),
故答案为:V(D)>V(C)>V(B)>V(A).
点评:本题考查过氧化氢分解的速率曲线,题目难度不大,主要考查浓度对反应速率的影响,注意对图象的分析.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
关于钠的叙述中,正确的是( )
| A、钠是银白色金属,硬度很大 |
| B、将金属钠放在坩埚里用酒精灯加热,生成淡黄色固体氧化钠 |
| C、金属钠在空气中燃烧,产生黄色火焰,生成过氧化钠 |
| D、金属钠的熔点很高 |
在“绿色化学”工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%.以下反应最符合绿色化学“原子经济性”要求的是( )
| A、乙烯聚合为聚乙烯高分子材料 |
| B、甲烷与氯气制备一氯甲烷 |
| C、乙醇与浓硫酸共热制备乙烯 |
| D、以苯和液溴为原料,在一定条件下生产溴苯 |
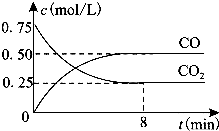 一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.