题目内容
19.工业上用铝土矿(主要成分为Al2O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如图: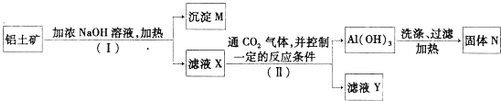
(1)Ⅰ和Ⅱ步骤中分离溶液和沉淀的操作是:过滤.
(2)沉淀M中除含有泥沙外,一定还含有Fe2O(填化学式),生成固体N反应的化学方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O.
(3)滤液X中,含铝元素的溶质的化学式为NaAlO2,它属于盐(填“酸”、“碱”或“盐”)类物质.
(4)实验室里常往AlCl3溶液中加入氨水(填“氨水”或“NaOH溶液”)来制取Al(OH)3,该反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(5)滤液Y中除了含有Na2CO3或NaHCO3外,一定还含有硅酸钠(或Na2SiO3).
分析 Fe2O3和氢氧化钠不反应,而氧化铝、二氧化硅能反应,步骤I利用过滤除去Fe2O3,沉淀M为氧化铁等不溶物,溶液X含有偏铝酸钠、硅酸钠,步骤II通入二氧化碳,控制条件使铝离子转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝,滤液Y含有硅酸盐、碳酸盐.
(1)分离固体与溶液的方法为过滤;
(2)由工艺流程可知,M为Fe2O3,N为Al2O3;
(3)溶液X含有偏铝酸钠,属于盐;
(4)氢氧化铝溶于强碱,实验室通常用弱碱氨水与铝盐制备氢氧化铝沉淀,氨水与氯化铝反应生成氢氧化铝与氯化铵;
(5)由流程可知滤液Y中除了含有Na2CO3或NaHCO3外,一定还含有硅酸钠.
解答 解:Fe2O3和氢氧化钠不反应,而氧化铝、二氧化硅能反应,步骤I利用过滤除去Fe2O3,沉淀M为氧化铁等不溶物,溶液X含有偏铝酸钠、硅酸钠,步骤II通入二氧化碳,控制条件使铝离子转化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝,滤液Y含有硅酸盐、碳酸盐.
(1)I和II步骤分离固体与溶液的方法为过滤;
故答案为:过滤;
(2)由工艺流程可知,M为Fe2O3,N为Al2O3,由氢氧化铝加热分解生成,方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,
故答案为:Fe2O3,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
(3)由工艺流程可知,滤液X中,含铝元素的溶质的化学式为:NaAlO2,属于盐,
故答案为:NaAlO2;盐;Al2O3+2NaOH=2NaAlO2+H2O、SiO2+2NaOH=Na2SiO3+H2O;
(4)氢氧化铝溶于强碱,实验室通常用弱碱氨水与铝盐制备氢氧化铝沉淀,氨水与氯化铝反应生成氢氧化铝与氯化铵,反应方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
故答案为:氨水;Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(5)溶液X含有偏铝酸钠、硅酸钠,步骤II通入二氧化碳,控制条件使铝离子转化为氢氧化铝沉淀,过滤得氢氧化铝,则滤液Y中除了含有Na2CO3或NaHCO3外,一定还含有硅酸钠,故答案为:硅酸钠(或Na2SiO3).
点评 本题以工艺流程题形式考查铝的化合物的性质、物质的分离提纯、处于化学用语书写等,为高频考点和常见题型,侧重于学生的分析能力和实验能力的考查,题目有利于培养学生良好的科学素养,难度中等,清楚工艺流程原理是关键,是对知识迁移的综合运用.

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
| A. | ②③④ | B. | ①②③ | C. | ③④⑤ | D. | ①④⑤ |
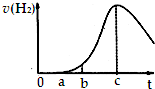 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )| A. | 曲线由0→a段发生了氧化还原反应 | |
| B. | 曲线由b→c段,产生氢气的速率增加较快的主要原因是反应放热 | |
| C. | c点达到了平衡 | |
| D. | c点以后,反应逐渐消耗了产生的氢气 |
| A. | KSCN溶液 | B. | NaOH溶液 | C. | AgNO3溶液 | D. | 溶液BaCl2 |
| X | Y | Z | |
| A | NaHCO3溶液 | Na2CO3 | Ba(OH)2溶液 |
| B | Fe2O3 | Al2O3 | NaOH溶液 |
| C | FeCl3溶液 | CuCl2 | Fe |
| D | Na2SO4溶液 | Na2CO3 | 盐酸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | ||
| C. | NaOH固体、CO2 | D. | 熔融的KNO3、硫酸溶液 |
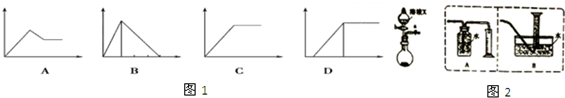
(1)如图1四个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量,从A~D中选择符合各题要求的序号填入表
| 溶液 | 加入的物质 | 答案序号 |
| AlCl3溶液 | 通入过量的NH3 | ① |
| 含少量NaOH的NaAlO2溶液 | 通过量的CO2 | ② |
| NaAlO2溶液 | 滴加稀H2SO4至过量 | ③ |
| MgCl2和AlCl3的混合液 | 滴加NaOH溶液至过量 | ④ |
实验步骤:
步骤1:连接装置并检查装置气密性;
步骤2:称取mg镁铝合金样品置于烧瓶中,在分液漏斗中盛放足量的溶液X;
步骤3:打开分液漏斗活塞b,使反应进行,待不再产生气泡时关闭活塞b;
步骤4:待装置冷却后,调平量筒与水槽的液面,读取气体体积为xmL(折合成标准状况下干燥气体的体积).
①测定氢气体积的装置选择A(填A或B)
②为了使合金中的铝与X反应,而Mg不反应,X应选用NaOH(填化学式),反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.③计算合金中铝的质量分数为$\frac{54x}{67.2m×1{0}^{3}}$(用m,x的代数式表示).
| A. | 分子中C、H、O的原子个数之比一定为1:4:4 | |
| B. | 一定为烃类 | |
| C. | 分子中一定含有氧原子 | |
| D. | 分子式为CH4Ox(x=0、1) |
 有机物的反应往往伴随副反应发生,因此需要分离提纯.有一种水果香精的合成步骤如下:
有机物的反应往往伴随副反应发生,因此需要分离提纯.有一种水果香精的合成步骤如下:Ⅰ合成:
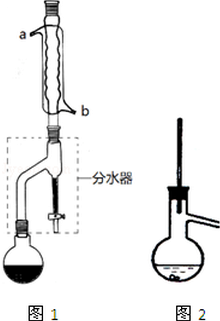
在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mL)正丁醇、7.2mL(7.5g,0.125mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好.在分水器中预先加入5.00mL水,其水面低于分水去回流支管下沿3~5mm,然后用小火加热,反应大约40min.
Ⅱ分离提纯:
①将烧瓶中反应后的混合物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10mL水、10mL10%碳酸钠溶液洗至无酸性(pH=7),充分震荡后静置,分去水层.
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥
③将乙酸正丁酯粗产品转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品,主要试剂及产物的物理常数如表:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
根据以上信息回答下列问题:
(1)合成和分离过程中均使用沸石,其作用防止液体加热时发生暴沸.
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从b(填a或b)管口通入.
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先过滤(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有正丁醚杂质.
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在bd中加热比较合适(请从下列选项中选择).
A.水 B.甘油(沸点290℃) C.沙子 D.石蜡油(沸点200~300℃)
(5)如何根据装置中的实验现象判断该合成反应达到了终点分水器中水面不再升高.
(6)反应结束后,若放出的水为6.98mL(水的密度为1g/mL),则正丁醇的利用率约为88%.