题目内容
9.在一定温度下的定容密闭容器中,当下列物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
| A. | ②③④ | B. | ①②③ | C. | ③④⑤ | D. | ①④⑤ |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①混合气体的压强一直不变,故错误; ②混合气体的密度不变,说明气体的质量不变,反应达平衡状态,故正确; ③B的物质的量浓度不变,说明正逆反应速率相等,反应达平衡状态,故正确; ④混合气体的平均相对分子质量不变,说明气体的质量不变,反应达平衡状态,故正确;⑤气体的总物质的量一直不变,故错误;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
17.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液 | 溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结. | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |
1.实验室用锌粒与2mol•L-1硫酸溶液制取氢气,下列措施能增大氢气产生速率的是( )
| A. | 将稀硫酸改成浓硫酸 | B. | 滴加少量硫酸钠溶液 | ||
| C. | 硫酸改成4 mol•L-1的醋酸 | D. | 滴加几滴硫酸铜溶液 |
18.电浮选凝聚法处理酸性污水的工作原理如图.下列说法正确的是( )
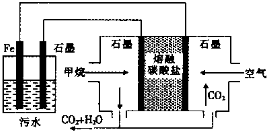

| A. | 左侧装置中的铁电极可换成石墨电极 | |
| B. | 通入甲烷的石墨电极的电极反应式为:CH4+4CO32--8e-═5CO2+2H2O | |
| C. | 通入空气的石墨电极做正极,发生氧化反应 | |
| D. | 若左侧装置中石墨电极产生标准状况下气体44.8L气体,则消耗2mol甲烷 |
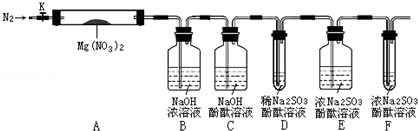
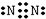 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.