题目内容
2.X、Y、Z是三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物.已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层.(1)X离子的结构示意图为
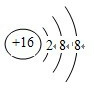 .
.(2)Z2Y对应水化物的碱性比LiOH强(填“强”或“弱”).
(3)Z2X属于离子(共价或离子)化合物.
(4)Z2Y2中含有离子键和共价键,Z2Y2溶于水时发生反应的化学方程式是2Na2O2+2H2O=4Na++4OH-+O2↑.
分析 由Z2Y、Z2Y2可推测是H2O、H2O2或Na2O、Na2O2,又因为Y离子和Z离子具有相同的电子层结构,所以只能是Na2O、Na2O2,由此知Z为Na,Y为O,由于XY2、XY3,可知X可形成?+4、+6价的化合物,且X离子比Y离子多1个电子层,X只能是S,结合对应物质的性质以及题目要求解答该题.
解答 解:由Z2Y、Z2Y2可推测是H2O、H2O2或Na2O、Na2O2,又因为Y离子和Z离子具有相同的电子层结构,所以只能是Na2O、Na2O2,由此知Z为Na,Y为O,由于XY2、XY3,可知X可形成?+4、+6价的化合物,且X离子比Y离子多1个电子层,X只能是S,
(1)X为S,S2-的离子结构示意图为 故答案为:
故答案为: ;
;
(2)Z2Y对应水化物为NaOH,因金属性Na>Li,则碱性NaOH较强,故答案为:强;
(3)Z2X为Na2O,为离子化合物,故答案为:离子;
(4)Na2O2含有离子键和共价键,与水反应生成氢氧化钠和氧气,方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:离子;共价;2Na2O2+2H2O=4Na++4OH-+O2↑.
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
12.某元素一种同位素的原子的质子数为m,中子数为n,则下列说法正确的是( )
| A. | 这种元素的原子量为m | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | (m+n)可写在该元素符号的左上角 | |
| D. | 核内中子的总质量小于质子的总质量 |
13.一定量的某饱和一元醛发生银镜反应,析出银21.6g,等量的此醛完全燃烧时生成CO2 8.96L(标况),则此醛是( )
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 2-甲基丁醛 |
10.某混合气体由两种气态烃组成,取2.24L该混合气体完全燃烧得到4.48L二氧化碳(气体体积已折算为标准状况)和3.6g水,则这两种气体可能是( )
| A. | CH4和C3H8 | B. | CH4和C3H4 | C. | C2H4和C2H6 | D. | C2H2和C2H6 |
7.下列物质中,既能与盐酸反应又能与NaOH溶液反应的是( )
①Ca(HCO3)2②Al(OH)3③NaAlO2④(NH4)2CO3 ⑤Al.
①Ca(HCO3)2②Al(OH)3③NaAlO2④(NH4)2CO3 ⑤Al.
| A. | ①④ | B. | ②③⑤ | C. | ①②④⑤ | D. | 全部 |
14.NA代表阿伏加罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,60gCH3COOH中含共用电子对数为7NA | |
| B. | 56g聚乙烯含有的碳原子数为4NA | |
| C. | 2molSO2和1molO2在密闭容器中充分反应后,容器内物质分子数等于2NA | |
| D. | 2L0.5mol/L乙酸溶液中H原子数为0.1NA |
11.键线式可以简明扼要地表示碳氢化合物,键线式为 的物质是( )
的物质是( )
 的物质是( )
的物质是( )| A. | 丙烷 | B. | 丁烷 | C. | 丙烯 | D. | 丁烯 |
12.分类是学习和研究化学的一种重要方法.下列分类不合理的是( )
| A. | Na2O、Na2O2都属于氧化物 | B. | H2SO4、CH3COOH都属于酸 | ||
| C. | 烧碱、纯碱都属于碱 | D. | Na2CO3、NaHCO3都属于盐 |
 .
.