题目内容
7.下列物质中,既能与盐酸反应又能与NaOH溶液反应的是( )①Ca(HCO3)2②Al(OH)3③NaAlO2④(NH4)2CO3 ⑤Al.
| A. | ①④ | B. | ②③⑤ | C. | ①②④⑤ | D. | 全部 |
分析 Al、Al2O3、Al(OH)3、弱酸酸式盐、弱酸的铵盐、氨基酸、蛋白质等都能和稀盐酸、NaOH反应,据此分析解答.
解答 解:①Ca(HCO3)2属于弱酸酸式盐,能和稀盐酸、NaOH反应生成盐和水,故正确;
②Al(OH)3属于两性氢氧化物,能和稀盐酸、NaOH反应生成盐和水,故正确;
③NaAlO2属于强碱弱酸盐,能和稀盐酸反应但不能和NaOH反应,故错误;
④(NH4)2CO3属于弱酸的铵盐,能和稀盐酸、NaOH反应,故正确;
⑤Al能和稀盐酸、NaOH反应生成盐和氢气,故正确;
故选C.
点评 本题考查元素化合物性质,为高频考点,明确元素化合物性质、物质之间的转化是解本题关键,注意基础知识的总结归纳,题目难度不大.

练习册系列答案
相关题目
17.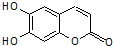 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A. | 2 mol Br2 2 mol NaOH | B. | 2 mol Br2 3 mol NaOH | ||
| C. | 3 mol Br2 4 mol NaOH | D. | 4 mol Br2 4 mol NaOH |
18.同分异构现象是有机物种类繁多的重要原因之一,下列互为同分异构体的一组化合物是( )
| A. | 甲烷和一氯甲烷 | B. | 淀粉和纤维素 | C. | 苯和甲苯 | D. | 蔗糖和麦芽糖 |
15.已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11,下列说法正确的是( )
| A. | 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)小 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 | |
| C. | 25℃时,在等体积等浓度的氨水、NH4Cl溶液中,Mg(OH)2的Ksp前者小于后者 | |
| D. | 25℃时,在MgF2的悬浊液中通入少量的HF气体,c(Mg2+)减小 |
12.化学与生活、生产、能源等密切相关,下列叙述不正确的是( )
| A. | 利用催化剂可将汽车尾气中的NO、CO转化为无毒的气体 | |
| B. | 化石燃料的过量使用加剧了雾霾天气及空气中的PM2.5 | |
| C. | 小苏打是制作馒头和面包的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 蛋白质溶液中加入饱和Na2SO4溶液或CuSO4溶液,析出固体原理相同 |
16.已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10.现向1L0.2mol/L的HF溶液中加入等体积等浓度的CaCl2溶液.下列说法正确的是( )
| A. | Ksp(CaF2)随浓度的变化而变化 | |
| B. | 上述混合体系中有CaF2沉淀生成 | |
| C. | 25℃时,0.1mol/L的HF溶液的pH=l | |
| D. | 上述反应的离子方程式为:Ca2++2F-=CaF2↓ |
17. 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.
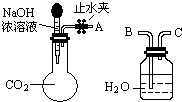
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
(3)在标况下,将4.48L CO2气体通入300mL 1mol/L 的NaOH的稀溶液中,写出该反应的离子方程式(用一个离子方程式表示)2CO2+3OH-=CO32-+HCO3-+H2O.
 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | 产生白色沉淀 | 有CO32- |
| ②过滤,取2mL滤液于试管中 | ||
| ③滴加酚酞 | 溶液变红 | 有OH- |
 .
.
 .
.