题目内容
12.某元素一种同位素的原子的质子数为m,中子数为n,则下列说法正确的是( )| A. | 这种元素的原子量为m | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | (m+n)可写在该元素符号的左上角 | |
| D. | 核内中子的总质量小于质子的总质量 |
分析 A.某元素一种同位素原子的质子数为m,中子数为n,只能确定该同位素的质量数;
B.无法计算该元素的相对原子质量;
C.元素符号的左上角数字表示质量数;
D.未知mn的关系,无法判断中子的总质量与质子的总质量大小.
解答 解:A.元素的相对原子质量与其核素及核素的丰度有关,原子的相对原子质量在数值上等于其质量数,所以该元素一种同位素原子的相对原子质量为m+n,而不是该元素的相对原子质量为m,故A错误;
B.题目已知某元素的一种核素的质子数和中子数,元素的相对原子质量与其核素及核素的丰度有关,该核素的丰度未知导致无法计算该元素的相对原子质量,故B正确;
C.某元素一种同位素原子的质子数为m,中子数为n,只能确定该元素一种同位素的质量数,不能由此确定该元素的质量数,故C错误;
D.未知mn的关系,核内中子的总质量可能小于也可能等于或大于质子的总质量,无法判断,故D错误;
故选B.
点评 本题考查了元素的相对原子质量的计算、核素的相对原子质量的计算等知识点,题目难度不大,明确元素和核素的相对原子质量的计算方法.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
13.分离以下三组混合物:①汽油和水 ②乙醇和水 ③碘和水,正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
20.下列物质属于电解质的是( )
| A. | 熔融的氯化钠 | B. | CO2 | C. | 食盐水 | D. | Fe |
7.1mol乙烯与Cl2完全加成,其产物再与Cl2彻底取代,两个过程中共用Cl2( )
| A. | 2mol | B. | 4mol | C. | 5mol | D. | 6mol |
17.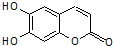 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A. | 2 mol Br2 2 mol NaOH | B. | 2 mol Br2 3 mol NaOH | ||
| C. | 3 mol Br2 4 mol NaOH | D. | 4 mol Br2 4 mol NaOH |
4.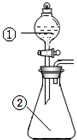 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硫酸 | 用砂纸打磨过的铝条 | 无明显现象 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 稀硝酸 | 铜片 | 立即产生大量红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
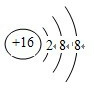
1.有5种元素X、Y、Z、Q、T.X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满.下列叙述不正确的是( )
| A. | 元素Y和Q可形成化合物Y2O3 | |
| B. | T和Z各有一种单质的空间构型为正四面体形 | |
| C. | X的最高价氧化物的立体构型为三角锥型 | |
| D. | ZO2是极性键构成的非极性分子,Z原子的杂化方式为sp杂化 |
 .
.