��Ŀ����
����X��Y��Z���ֳ���������Ԫ�أ�Y��ZΪͬ���ڽ���Ԫ�أ���X��Y��ij�ֻ�����Ϊ����ɫ����M��Y��Z������������Ӧ��ˮ������Է�Ӧ������N��ˮ������˵������ȷ���ǣ�������
| A������M����ˮ��Ӧ����X���ʺ�һ��ǿ�� |
| B��Z���ʵı�Ƭ�ھƾ����ϼ������ۻ����������� |
| C��Y������������Ӧ��ˮ�������N��������ˮ�ĵ��� |
| D��M��N�о��������Ӽ����ۼ� |
���㣺ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
��������X��Y��Z���ֳ���������Ԫ�أ���X��Y��ij�ֻ�����Ϊ����ɫ����M����MΪNa2O2��X��Y�ֱ�ΪNa��O�е�һ�֣�Y��ZΪͬ���ڽ���Ԫ�أ�����֪YΪNa��XΪO����Y��Z������������Ӧ��ˮ������Է�Ӧ������N��ˮ����ZΪAl��NΪNaAlO2���ݴ˽��
���
�⣺��X��Y��Z���ֳ���������Ԫ�أ���X��Y��ij�ֻ�����Ϊ����ɫ����M����MΪNa2O2��X��Y�ֱ�ΪNa��O�е�һ�֣�Y��ZΪͬ���ڽ���Ԫ�أ�����֪YΪNa��XΪO����Y��Z������������Ӧ��ˮ������Է�Ӧ������N��ˮ����ZΪAl��NΪNaAlO2��
A��MΪNa2O2����ˮ��Ӧ����������������������A��ȷ��
B��Al���ʵı�Ƭ�ھƾ����ϼ��ȣ�����������������Ĥ���������۵�Ƚ�Al�ߣ��ʼ���ʱ�ۻ����������䣬��B��ȷ��
C��Y������������Ӧ��ˮ����ΪNaOH��������ˮ�ĵ��룬NΪNaAlO2������Һ�з���ˮ�⣬�ܴٽ�ˮ�ĵ��룬��C����
D��Na2O2��NaAlO2���������ӻ�������������Ӽ������������й���������ԭ��֮���γɹ��ۼ���ƫ��������ƫ������д��ڹ��ۼ�����D��ȷ��
��ѡC��
A��MΪNa2O2����ˮ��Ӧ����������������������A��ȷ��
B��Al���ʵı�Ƭ�ھƾ����ϼ��ȣ�����������������Ĥ���������۵�Ƚ�Al�ߣ��ʼ���ʱ�ۻ����������䣬��B��ȷ��
C��Y������������Ӧ��ˮ����ΪNaOH��������ˮ�ĵ��룬NΪNaAlO2������Һ�з���ˮ�⣬�ܴٽ�ˮ�ĵ��룬��C����
D��Na2O2��NaAlO2���������ӻ�������������Ӽ������������й���������ԭ��֮���γɹ��ۼ���ƫ��������ƫ������д��ڹ��ۼ�����D��ȷ��
��ѡC��
���������⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���X��Y��ij�ֻ�����Ϊ����ɫ�������ƶ�ͻ�ƿڣ���Ҫѧ���������ջ���֪ʶ���ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
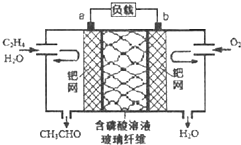 ��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ������Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦΪ��CH2=CH2+O2��2CH3CHO�������й�˵����ȷ���ǣ�������
��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ������Ʊ���ȩ��ͬʱ��õ��ܣ����ܷ�ӦΪ��CH2=CH2+O2��2CH3CHO�������й�˵����ȷ���ǣ�������| A���õ��Ϊ�ɳ���� |
| B��ÿ��0.1mol O2��Ӧ����Ǩ��H+0.4mol |
| C��������ӦʽΪ��CH2=CH2-2e-+2OH-�TCH3CHO+H2O |
| D�������ƶ����缫a��������Һ���缫b |
����˵����ȷ�ģ�������
| A�����ع��͡������ܻ��������ڱ��������������ʣ������ڸ߷��ӻ�������Խ����к� |
| B��������ˮʱ�����˻�ѧ�������仯������ɱ�������������� |
| C�������Ѿƴ���ʱ�䳤���������Ϊ�Ҵ�������������Ӧ |
| D�����ơ����Ƚ���Ԫ�ص�������Ѥ������ɫ��������������� |
�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�̨��������Һ��pH���±���
�����жϲ���ȷ���ǣ�������
| ʵ���� | HA���ʵ���Ũ�ȣ�mol?L-1�� | NaOH���ʵ���Ũ�ȣ�mol?L-1�� | �����Һ��pH |
| �٢ڢ� | 0.1 | 0.1 | pH=9 |
| C | 0.2 | pH=7 | |
| 0.2 | 0.1 | pH��7 |
| A��HA�ĵ��뷽��ʽΪ��HA?H++A- |
| B���������������ʵ������c��0.2 |
| C������ʵ���У������Һ��c��A-����c��Na+����c��HA����c��H+����c��OH-�� |
| D������ʵ���У������Һ��c��A-��=��0.1+10-9-10-5��mol/L |
 ��CO2��һ����������H2��Ӧת��Ϊ�״���CH4O���DZ��Ϊ���ĺ÷�����һ�������£�ÿת��1kg CO2�ų�������Ϊ1113.64KJ��CO2ת��Ϊ�״�������Ũ����ʱ��ı仯������ͼ��ʾ����֪��Ӧ����������ڴ������¾�Ϊ���壩��������������ȷ���ǣ�������
��CO2��һ����������H2��Ӧת��Ϊ�״���CH4O���DZ��Ϊ���ĺ÷�����һ�������£�ÿת��1kg CO2�ų�������Ϊ1113.64KJ��CO2ת��Ϊ�״�������Ũ����ʱ��ı仯������ͼ��ʾ����֪��Ӧ����������ڴ������¾�Ϊ���壩��������������ȷ���ǣ�������| A���ڽ��е�3����ʱ��CO2��H2������ķ�Ӧ����ֵ��ȣ���Ϊ0.5mol?L-1?min-1 | ||
| B���˷�Ӧ���Ȼ�ѧ����ʽΪ��CO2��g��+3H2��g��?CH4O��g��+H2O��g����H=-49.0KJ/mol | ||
C���������·�Ӧ��ƽ�ⳣ��Ϊ
| ||
| D�������¶ȣ��˷�Ӧ��ƽ�ⳣ������Ϊ0.8 |
����˵����ȷ���ǣ�������
| A���ױ��DZ�����������ϩ�Dz������� |
| B��ʯ�͵��ѻ���Ʒ��ʹ��ˮ��ɫ |
| C����������CuSO4��Һ�з������� |
| D����֬��NaOH��Һ��ˮ�����ɸ�֬������� |
�����£���0.01mol?L-1 Na2SO3��Һ��0.01mol?L-1 KHSO3��Һ�������ϣ������Ի�Ϻ���Һ������ı仯���������ж���ȷ������������
| A����Ϻ���Һ�д����й�ϵ��C��K+��+C��Na+��+C��H+��=C��SO32-��+C��HSO3-��+C��OH-�� |
| B����Ϻ���Һ�д����й�ϵ��C��K+��+C��H2SO3��+C��H+��=C��SO32-��+C��OH-�� |
| C����Ϻ���Һ�д����й�ϵ��C��SO32-��+C��HSO3-��+C��H2SO3��=0.02 mol?L-1 |
| D������Һ���ǰ��Na2SO3��Һ��ˮ�����C��H+��С��KHSO3��Һ��ˮ�����C��H+�� |
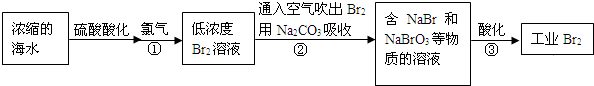
 �������糧�ͷų������������NOx����SO2��CO2���������ɻ������⣮��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ģ�
�������糧�ͷų������������NOx����SO2��CO2���������ɻ������⣮��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ģ�