题目内容
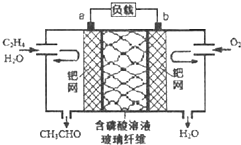 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )| A、该电池为可充电电池 |
| B、每有0.1mol O2反应,则迁移H+0.4mol |
| C、正极反应式为:CH2=CH2-2e-+2OH-═CH3CHO+H2O |
| D、电子移动方向:电极a→磷酸溶液→电极b |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:由总反应式可知CH2=CH2被氧化,应为原电池的负极反应,因电解质溶液呈酸性,则负极电极方程式为CH2=CH2-2e-+H2O=CH3CHO+2H+,正极通入氧气,发生还原反应,电极方程式为O2+4H++4e-═2H2O,以此解答该题.
解答:
解:A.充电时,不能生成乙烯和氧气,不是充电电池,故A错误;
B.由电极方程式O2+4H++4e-═2H2O可知,每有0.1mol O2反应,则迁移H+0.4mol,故B正确;
C.正极发生还原反应,电极方程式为O2+4H++4e-═2H2O,负极为CH2=CH2-2e-+H2O=CH3CHO+2H+,故C错误;
D.电子只能经过导线,不能经过溶液,故D错误.
故选B.
B.由电极方程式O2+4H++4e-═2H2O可知,每有0.1mol O2反应,则迁移H+0.4mol,故B正确;
C.正极发生还原反应,电极方程式为O2+4H++4e-═2H2O,负极为CH2=CH2-2e-+H2O=CH3CHO+2H+,故C错误;
D.电子只能经过导线,不能经过溶液,故D错误.
故选B.
点评:本题考查了原电池原理的应用,为高频考点,注意掌握电极方程式的书写是解决本题的关键,易错点为D,注意电子不能流经溶液,题目难度中等.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1 mol?L-1 Fe(NO3)2溶液:Mg2+、H+、SO42-、Cl- |
| B、0.1 mol?L-1 Ag(NH3)2OH溶液:Na+、H+、Cl-、NO3- |
| C、与金属铝能产生大量H2的溶液:K+、Na+、HCO3-、NO3- |
| D、c(H+)+c(OH-)=2×10-7mol?L-1的溶液:K+、Na+、Br-、Cl- |
含有下列各组离子的溶液中,通入过量SO2气体后仍能大量共存的是( )
| A、H+、Ca2+、Fe3+、NO3- |
| B、Ba2+、ClO-、Na+、OH- |
| C、Na+、NH4+、I-、HS- |
| D、Na+、Ca2+、K+、Cl- |
铋(Bi)在医药方面有重要应用,下列关于
Bi和
Bi的说法正确的是( )
209 83 |
210 83 |
| A、两者互为同素异形体 | ||||
B、
| ||||
C、
| ||||
| D、两者分别含有126和127个质子 |
下列说法不正确的是( )
| A、汽车尾气中有NOx,主要是汽油不充分燃烧引起的 |
| B、日用铝制品表面覆盖着氧化膜,对金属起保护作用 |
| C、实验室常用粗锌和稀硫酸反应制取H2 |
| D、从海水中提取溴的过程涉及氧化还原反应 |
下列离子方程式表达正确的是( )
| A、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| C、向H2O中投入少量Na218O2固体:2H2O+2Na218O2═4Na++418 OH-+O2↑ |
| D、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
下列有关物质性质的应用正确的是( )
| A、常温下干燥氯气与铁不反应,可以用钢瓶储存氯水 |
| B、铜的金属活泼性比铁的弱,可在铁船闸上装若干铜块以减缓其腐蚀 |
| C、二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
| D、次氯酸钠具有强氧化性,可用于配制消毒液 |
以下性质的比较可能错误的是( )
| A、离子半径 H->Li+ |
| B、熔点 Al2O3>MgO |
| C、结合质子(H+)的能力 CO32->ClO- |
| D、密度 1-氯戊烷>1-氯己烷 |
现有X、Y、Z三种常见短周期元素,Y、Z为同周期金属元素,且X和Y的某种化合物为淡黄色固体M,Y、Z的最高价氧化物对应的水化物可以反应生成盐N和水.下列说法不正确的是( )
| A、固体M能与水反应生成X单质和一种强碱 |
| B、Z单质的薄片在酒精灯上加热能熔化,但不滴落 |
| C、Y的最高价氧化物对应的水化物和盐N均能抑制水的电离 |
| D、M和N中均含有离子键和共价键 |