题目内容
14.实验室制备Al2S3,下列方案可行的是( )| A. | 将AlCl3溶液与Na2S溶液混合 | B. | 将H2S气体通入Al2(SO4)3溶液中 | ||
| C. | 将Al(NO3)3固体与K2S固体混合 | D. | 将金属铝与硫混合加热 |
分析 A.铝离子与硫离子发生双水解反应生成氢氧化铝沉淀,无法获得硫化铝;
B.硫化氢气体不与硫酸铝发生反应;
C.硝酸铝不与硫化钾固体反应;
D.金属铝与硫单质加热反应生成硫化铝.
解答 解:A.由于Al2S3在水溶液中易发生水解相互促进的反应,生成Al(OH)3和H2S,则不能用AlCl3溶液与Na2S溶液混合制取硫化铝,故A错误;
B.将H2S气体通入Al2(SO4)3溶液中不发生反应,无法制取硫化铝,故B错误;
C.将Al(NO3)3固体与K2S固体混合不会发生反应,故C错误;
D.加热铝和硫单质能够发生反应生成硫化铝,故D正确;
故选D.
点评 本题考查了物质制备方案的设计与评价,题目难度不大,明确硫化铝在水溶液中发生水解反应为解答关键,注意熟练掌握常见元素及其化合物性质,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
12.下列事实一定能说明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验灯泡很暗
③HNO2和NaCl不能发生反应
④0.1mol/LHNO2溶液的pH=2.1.
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验灯泡很暗
③HNO2和NaCl不能发生反应
④0.1mol/LHNO2溶液的pH=2.1.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
6.丁醇(C4H10O)与乙二酸(HOOC-COOH)在一定条件下反应,生成的二元酯有( )
| A. | 4种 | B. | 8种 | C. | 10种 | D. | 16种 |
3.下列变化过程中,不需要破坏化学键的是( )
| A. | 食盐溶于水 | B. | 碘的升华 | ||
| C. | 氯气溶于氢氧化钠溶液 | D. | 氢氧化钠受热熔化 |
4.一种熔融碳酸盐燃料电池的工作原理如图所示.下列有关该电池说法正确的是( )
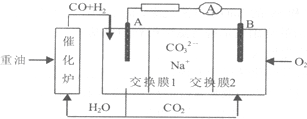

| A. | 重油是石油分馏的产品,含有的主要元素为C、H、O | |
| B. | 电极B上发生的电极反应为:O2+2CO2+4e-═2CO32- | |
| C. | 电极A上H2参与的电极反应为:H2+2OH--2e-═2H2O | |
| D. | 电池工作时,CO32-向电极B移动 |
 .
.