题目内容
9.分析下列化学式,选出符合要求的物质填空,要求填写化学式.A、N2 B、CO2 C、CH2Cl2 D、C2H4 E、C2H6
上述物质中,只含有极性键的分子是C;既含离子键又含共价键的化合物是DE;只存在σ键的是CE;既有σ键,又有π键的是ABD.
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,共价单键为σ键,双键和三键中均含1个π键,以此来解答.
解答 解:A、N2含N≡N,为单质,只含非极性键,既有σ键,又有π键;
B、CO2的结构式为O=C=O,只含极性键,既有σ键,又有π键;
C、CH2Cl2中只含极性键,均为单键,则只含σ键;
D、C2H4的结构简式为CH2=CH2,含极性键和非极性键,既有σ键,又有π键;
E、C2H6中含极性键和非极性键,均为单键,则只含σ键;
则上述物质中,只含有极性键的分子是C;既含极性键又含非极性共价键的化合物是DE;只存在σ键的是CE;既有σ键,又有π键的是ABD,
故答案为:C;DE;CE;ABD.
点评 本题考查共价键,为高频考点,把握化学键的形成及判断是的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质的化学键及共价键类型,题目难度不大.

练习册系列答案
相关题目
6.如表中的实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向含有KSCN溶液的FeSO4溶液中滴加硫酸酸化的H2O2溶液 | 检验H2O2的氧化性大于Fe3+ |
| B | 滴入KI试液 | 检验淀粉是否已完全水解 |
| C | 先滴入Ba(NO3)2溶液.产生沉淀,加入足量稀盐酸,仍有沉淀 | 检验溶液中是否含有SO42- |
| D | 向乙醇溶液加入钠粒 | 测定乙醇分子中含有羟基 |
| A. | A | B. | B | C. | C | D. | D |
7.下列图示中,属于蒸馏操作的是( )
| A. |  | B. |  | ||
| C. | 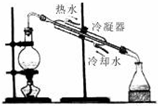 | D. |  |
4.N2和O2组成的混合气体,其平均相对分子质量为29,则混合气体中,N2和O2的物质的量之比为( )
| A. | 3:1 | B. | 2:1 | C. | 1:1 | D. | 1:3 |
4.一些科学家预言存在稳定的超重元素,如N=184的原子,它位于元素周期表第七周期,ⅣA族.由此,下列说法正确的是( )
| A. | 该原子核外有114个电子 | B. | 该原子的质子数是184 | ||
| C. | 第七周期有50种元素 | D. | 该元素的相对原子质量是298 |
14.实验室制备Al2S3,下列方案可行的是( )
| A. | 将AlCl3溶液与Na2S溶液混合 | B. | 将H2S气体通入Al2(SO4)3溶液中 | ||
| C. | 将Al(NO3)3固体与K2S固体混合 | D. | 将金属铝与硫混合加热 |
1.肼(N2H4)可以用如下方法制备:CO(NH2)2+ClO-+OH--N2H4+Cl-+CO32-+H2O[CO(NH2)2中N为-3价],下列说法不正确的是( )
| A. | N2H4是氧化产物 | |
| B. | 配平后,OH-的化学计量数是2 | |
| C. | 生成3.2g N2H4 转移0.1mol 电子 | |
| D. | 氧化剂与还原剂物质的量之比为1:1 |
18.向20mL 2mol/L AlCl3溶液中加入30mL 5mol/L的NaOH溶液,充分反应后得到白色沉淀,则白色沉淀的质量为( )
| A. | 3.12g | B. | 3.9g | C. | 0.78g | D. | 2.34g |
19.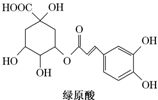 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )| A. | 奎尼酸分子式为C7H12O6 | |
| B. | 绿原酸能发生取代、加成、消去和缩聚反应 | |
| C. | 1mol奎尼酸与NaOH溶液反应,最多消耗5mol NaOH | |
| D. | 咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应 |