题目内容
新型NaBH4/H2O2燃料电池(DBFC)的结构如图所示,该电池总反应方程式:NaBH4+4H2O2═NaBO2+6H2O,有关的说法不正确的是( )
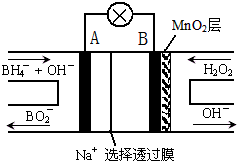

| A、电极B为正极 |
| B、放电过程中,Na+从正极区向负极区迁移 |
| C、电池负极的电极反应为:BH4-+8OH--8e-═BO2-+6H2O |
| D、在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12NA |
考点:化学电源新型电池
专题:
分析:该燃料电池中,根据元素化合价变化知,负极上电极反应式为BH4-+8OH--8e-=BO2-+6H2O,正极H2O2发生还原反应,得到电子被还原生成OH-,电极反应式为H2O2+2e-=2OH-,放电时,阳离子向正极移动、阴离子向负极移动,根据双氧水和转移电子之间的关系式计算.
解答:
解:A.根据图片知,B电极上双氧水得电子生成氢氧根离子,所以B电极是正极,故A正确;
B.放电时,阳离子向正极移动、阴离子向负极移动,所以Na+从负极区向正极区迁移,故B错误;
C.根据元素化合价变化知,负极上BH4-失电子发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故C正确;
D.在电池反应中,每消耗1L 6mol/L H2O2溶液,消耗双氧水的物质的量为6mol,根据知H2O2+2e-=2OH-,理论上流过电路中的电子数=
×2×NA/mol=12NA,故D正确;
故选B.
B.放电时,阳离子向正极移动、阴离子向负极移动,所以Na+从负极区向正极区迁移,故B错误;
C.根据元素化合价变化知,负极上BH4-失电子发生氧化反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,故C正确;
D.在电池反应中,每消耗1L 6mol/L H2O2溶液,消耗双氧水的物质的量为6mol,根据知H2O2+2e-=2OH-,理论上流过电路中的电子数=
| 6mol |
| 1 |
故选B.
点评:本题考查原电池原理,明确正负极与元素化合价变化关系是解本题关键,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,题目难度中等.

练习册系列答案
相关题目
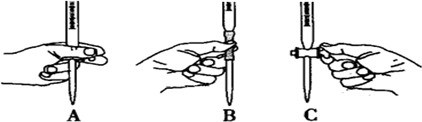
下列实验基本操作中,正确的是( )
A、 |
B、 |
C、 |
D、 |

 ,
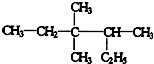
,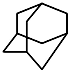 .的分子式为
.的分子式为