��Ŀ����
���淴ӦA��g��+B��g��?C��g��+D��g��+2E��s����2L���ܱ������н�����ƽ�⣮���¶�Ϊ749Kʱ��K=
���ʣ�
��1����A��B����ʼŨ��Ϊ2mol/Lʱ��A��ת����Ϊ ����A����ʼŨ�Ƚ�Ϊ1mol/L��B����ʼŨ�����Ϊ3mol/Lʱ��A��ת���� ���������С�����䡱��
��2��������ͬ�������£���ͬһ�����и�Ϊ1molA��1molB��1molC��1molD��3molE��ﵽƽ��ʱC�����ʵ����� ��
��3�����������¶�Ϊ500K��ʼ�����ʵ�����Ϊ4molʱ����ƽ��ʱC�����ʵ���Ϊ2mol����÷�Ӧ�ķ�Ӧ�� 0�����������������=������
������һ��ʱ�����������C��g�������ʵ�����Ũ�ȵ���
a�������¶ȡ�b��ѹ��������� c��������� d������A������ e���Լ���E������
| 9 |
| 4 |
��1����A��B����ʼŨ��Ϊ2mol/Lʱ��A��ת����Ϊ
��2��������ͬ�������£���ͬһ�����и�Ϊ1molA��1molB��1molC��1molD��3molE��ﵽƽ��ʱC�����ʵ�����
��3�����������¶�Ϊ500K��ʼ�����ʵ�����Ϊ4molʱ����ƽ��ʱC�����ʵ���Ϊ2mol����÷�Ӧ�ķ�Ӧ��
������һ��ʱ�����������C��g�������ʵ�����Ũ�ȵ���
a�������¶ȡ�b��ѹ��������� c��������� d������A������ e���Լ���E������
���㣺��ѧƽ��ļ���,��ѧƽ���Ӱ������
ר�⣺
��������1�����ݻ�ѧƽ������ʽ��ƽ�ⳣ���������ʽ��ʽ���㣬ת����=
��100%�����ַ�Ӧ������һ������������������һ�����ʵ�ת���ʣ�
��2�����ݻ�ѧƽ������ʽ���ƽ�ⳣ�����㣻
��3�����ݻ�ѧƽ�ⳣ������ƽ�ⳣ�����Ƚ�ƽ�ⳣ���仯�����жϷ�Ӧ�����仯�����������C��g�������ʵ�����Ũ�ȵĿ��Ըı�����ƽ��������л�����C��Ũ�ȣ�
| ������ |
| ��ʼ�� |
��2�����ݻ�ѧƽ������ʽ���ƽ�ⳣ�����㣻
��3�����ݻ�ѧƽ�ⳣ������ƽ�ⳣ�����Ƚ�ƽ�ⳣ���仯�����жϷ�Ӧ�����仯�����������C��g�������ʵ�����Ũ�ȵĿ��Ըı�����ƽ��������л�����C��Ũ�ȣ�
���
�⣺��1����A���������ʵ���Ũ��Ϊx
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol/L�� 2 2 0 0
�仯����mol/L�� x x x x
ƽ������mol/L�� 2-x 2-x x x
K=
=
x=1.2mol/L
Aת����=
��100%=
��100%=60%�����ַ�Ӧ������һ������������������һ�����ʵ�ת���ʣ���A����ʼŨ�Ƚ�Ϊ1mol/L��B����ʼŨ�����Ϊ3mol/Lʱ��A��ת��������
�ʴ�Ϊ��60%������
��2��������ͬ�������£���ͬһ�����и�Ϊ1molA��1molB��1molC��1molD��3molE��
����Ũ����Q=
=1��K����Ӧ������У��������������C���ʵ���Ϊy
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol�� 1 1 1 1
�仯����mol�� y y y y
ƽ������mol�� 1-y 1-y 1+y 1+y
K=
=
y=0.2mol
��ﵽƽ��ʱC�����ʵ�����1.2mol��
�ʴ�Ϊ��1.2mol��
��3�����ݻ�ѧƽ�ⳣ������ƽ�ⳣ�����Ƚ�ƽ�ⳣ���仯�����жϷ�Ӧ�����仯��
���������¶�Ϊ500K��ʼ�����ʵ�����Ϊ4molʱ����ƽ��ʱC�����ʵ���Ϊ2mol
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol�� 4 4 0 0
�仯����mol�� 2 2 2 2
ƽ������mol�� 2 2 2 2
��Ӧǰ��������ڲ��䣬��ƽ�ⳣ�����������������ʵ�������K=
=1������ƽ�ⳣ����С˵��ƽ��������У��淴ӦΪ���ȷ�Ӧ������Ӧ Ϊ���ȷ�Ӧ����H��0��
���������C��g�������ʵ�����Ũ�ȵĿ��Ըı�����ƽ��������л�����C��Ũ�ȣ���Ӧ�����������������ȷ�Ӧ��
a�������¶�ƽ��������У�C���ʵ���Ũ������a��ȷ��
b��ѹ�������������ѹǿƽ�ⲻ����C���ʵ������䣬Ũ������b��ȷ��
c������������ı仯ѧƽ�⣬��Ӧ��������C���ʵ���Ũ�� ���䣬��c����
d������A��������ƽ��������У�CŨ������d��ȷ��
e��EΪ���壬�Լ���E������ƽ�ⲻ�䣬CŨ�Ȳ��䣬��e����
�ʴ�Ϊ������abd��
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol/L�� 2 2 0 0
�仯����mol/L�� x x x x
ƽ������mol/L�� 2-x 2-x x x
K=
| x2 |
| (2-x)2 |
| 9 |
| 4 |
x=1.2mol/L
Aת����=
| ������ |
| ��ʼ�� |
| 1.2mol/L |
| 2mol/L |
�ʴ�Ϊ��60%������
��2��������ͬ�������£���ͬһ�����и�Ϊ1molA��1molB��1molC��1molD��3molE��
����Ũ����Q=
| 1��1 |
| 1��1 |
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol�� 1 1 1 1
�仯����mol�� y y y y
ƽ������mol�� 1-y 1-y 1+y 1+y
K=
| (1+y)2 |
| (1-y)2 |
| 9 |
| 4 |
y=0.2mol
��ﵽƽ��ʱC�����ʵ�����1.2mol��
�ʴ�Ϊ��1.2mol��
��3�����ݻ�ѧƽ�ⳣ������ƽ�ⳣ�����Ƚ�ƽ�ⳣ���仯�����жϷ�Ӧ�����仯��
���������¶�Ϊ500K��ʼ�����ʵ�����Ϊ4molʱ����ƽ��ʱC�����ʵ���Ϊ2mol
A��g��+B��g��?C��g��+D��g��+2E��s��
��ʼ����mol�� 4 4 0 0
�仯����mol�� 2 2 2 2
ƽ������mol�� 2 2 2 2
��Ӧǰ��������ڲ��䣬��ƽ�ⳣ�����������������ʵ�������K=
| 2��2 |
| 2��2 |
���������C��g�������ʵ�����Ũ�ȵĿ��Ըı�����ƽ��������л�����C��Ũ�ȣ���Ӧ�����������������ȷ�Ӧ��
a�������¶�ƽ��������У�C���ʵ���Ũ������a��ȷ��
b��ѹ�������������ѹǿƽ�ⲻ����C���ʵ������䣬Ũ������b��ȷ��
c������������ı仯ѧƽ�⣬��Ӧ��������C���ʵ���Ũ�� ���䣬��c����
d������A��������ƽ��������У�CŨ������d��ȷ��
e��EΪ���壬�Լ���E������ƽ�ⲻ�䣬CŨ�Ȳ��䣬��e����
�ʴ�Ϊ������abd��
���������⿼���˻�ѧƽ��������㣬ת���ʡ�ƽ�ⳣ������Ӧ ���ʸ���ļ���Ӧ�ã�Ӱ��ƽ������ط����жϣ����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д�
�����Ŀ
����NaBH4/H2O2ȼ�ϵ�أ�DBFC���Ľṹ��ͼ��ʾ���õ���ܷ�Ӧ����ʽ��NaBH4+4H2O2�TNaBO2+6H2O���йص�˵������ȷ���ǣ�������
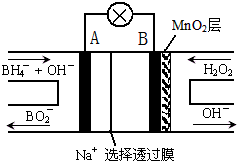

| A���缫BΪ���� |
| B���ŵ�����У�Na+������������Ǩ�� |
| C����ظ����ĵ缫��ӦΪ��BH4-+8OH--8e-�TBO2-+6H2O |
| D���ڵ�ط�Ӧ�У�ÿ����1L 6mol/L H2O2��Һ��������������·�еĵ���Ϊ12NA |
����˵����ȷ���ǣ�������
| A����NaH����ˮ���õ���ˮ��Һ�ܵ���˵��NaH�����ӻ����� |
| B��Fe��OH��3�����Fe��OH��3�����Ļ�ѧ���ʲ���ͬ |
| C���Ҵ������к��ǻ�����������Ʒ�Ӧ�������� |
| D��MnO2���н�ǿ�����ԣ�����ΪH2O2�ֽⷴӦ�������� |
25��ʱ��ˮ�����ӻ�ΪK�����¶��½�a mol?L-1������b mol?L-1��ˮ�������ϣ���ǡ����ȫ��Ӧ�����н����в���ȷ���ǣ�������
A�����Һ�У�c��H+����
| ||
| B�����Һ�У�c��NH3H2O��+c��NH4+��=0.5a mol?L-1 | ||
| C��a=b | ||
| D�����Һ�У�c��H+��+c��NH4+��=c��OH-��+c��Cl-�� |