题目内容
通过实验测定反应速率的方法有多种,如:
①比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的 来实现;
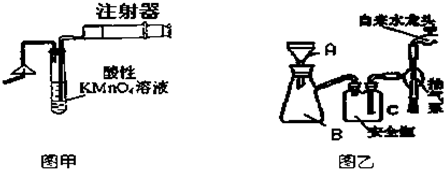
②在KMnO4与H2C2O4反应中,KMnO4与H2C2O4反应的离子方程式: .可通过测定 来测定该反应的速率;
③在Na2S2O3和H2SO4反应中,反应方程式为: 该反应的速率可通过 来测定.
①比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的
②在KMnO4与H2C2O4反应中,KMnO4与H2C2O4反应的离子方程式:
③在Na2S2O3和H2SO4反应中,反应方程式为:
考点:测定某些化学反应的速率
专题:化学反应速率专题
分析:通过测定收集等体积H2需要的时间来测定锌粒与不同浓度硫酸反应时的速率;
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,反应后,溶液由紫红色变为无色,故可通过测定溶液褪色所需时间来测定该反应的速率;
Na2S2O3和H2SO4发生氧化还原反应,生成单质硫,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率.
KMnO4与H2C2O4发生氧化还原反应,生成锰离子、水和二氧化碳,反应后,溶液由紫红色变为无色,故可通过测定溶液褪色所需时间来测定该反应的速率;
Na2S2O3和H2SO4发生氧化还原反应,生成单质硫,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率.
解答:
解:①通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的时间来实现;故答案为:时间;
②在KMnO4与H2C2O4反应中,高锰酸钾具有强氧化性,能将草酸氧化:2MnO4-+5H2C2O4+6H+=2Mn2++8H2O+10CO2↑,反应后,溶液的紫红色颜色会消失,故可通过测定溶液褪色所需时间来测定该反应的速率;
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++8H2O+10CO2↑;溶液褪色所需时间;
③Na2S2O3和H2SO4反应为:Na2S2O3+H2S04=Na2SO4+SO2↑+S↓+H2O,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率;
故答案为:Na2S2O3+H2S04=Na2SO4+SO2↑+S↓+H2O;出现浑浊的时间.
②在KMnO4与H2C2O4反应中,高锰酸钾具有强氧化性,能将草酸氧化:2MnO4-+5H2C2O4+6H+=2Mn2++8H2O+10CO2↑,反应后,溶液的紫红色颜色会消失,故可通过测定溶液褪色所需时间来测定该反应的速率;
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++8H2O+10CO2↑;溶液褪色所需时间;
③Na2S2O3和H2SO4反应为:Na2S2O3+H2S04=Na2SO4+SO2↑+S↓+H2O,反应后,有淡黄色沉淀生成,故可通过出现浑浊的时间来测定该反应的速率;
故答案为:Na2S2O3+H2S04=Na2SO4+SO2↑+S↓+H2O;出现浑浊的时间.
点评:本题考查反应速率的测定方法,难度不大.要注意通过实验测定反应速率的方法有多种,测定时间是其中的一种.

练习册系列答案
相关题目
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、碱 纯碱 NaOH |
| B、酸性氧化物 干冰 CO |
| C、酸 硫酸 H2S |
| D、盐 纯碱 Na2CO32 |
新型NaBH4/H2O2燃料电池(DBFC)的结构如图所示,该电池总反应方程式:NaBH4+4H2O2═NaBO2+6H2O,有关的说法不正确的是( )
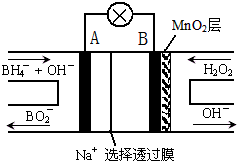

| A、电极B为正极 |
| B、放电过程中,Na+从正极区向负极区迁移 |
| C、电池负极的电极反应为:BH4-+8OH--8e-═BO2-+6H2O |
| D、在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12NA |
下列说法正确的是( )
| A、将NaH溶于水,得到的水溶液能导电说明NaH是离子化合物 |
| B、Fe(OH)3胶体和Fe(OH)3沉淀的化学性质不相同 |
| C、乙醇分子中含羟基,可与金属钠反应生成氢气 |
| D、MnO2具有较强氧化性,可作为H2O2分解反应的氧化剂 |