题目内容
某学生欲用已知物质的量浓度的醋酸来测定未知物质的量浓度的氢氧化钠溶液时,选择适当的指示剂.请填写下列空白:
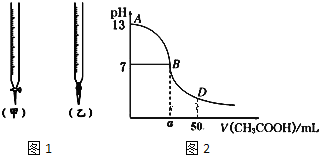
(1)用标准醋酸滴定待测的氢氧化钠溶液时,从上属选项中选出最恰当的一项 .滴定时应左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 .直到加入最后一滴醋酸,溶液颜色由 为止.
(2)下列操作中可能使所测氢氧化钠溶液的浓度值偏低的是 .
A.酸式滴定管未用标准醋酸润洗就直接注入标准醋酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取醋酸体积时,开始仰视读数,滴定结束后俯视读数
(3)某学生根据3次实验分别记录有关数据如表:
依据上表数据列式计算该氢氧化钠溶液的物质的量浓度为 .
(4)如图2为上述25mL NaOH溶液中逐滴滴加CH3COOH溶液过程中溶液pH的变化曲线.请回答:
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间.(若正确,此问不答).
②在AB区间内,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)的大小关系是 .
A.c(OH-)一定大于c(CH3COO-) B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)可能等于c(CH3COO-)
③在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+).(填“>”、“<”或“=”)

| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
(2)下列操作中可能使所测氢氧化钠溶液的浓度值偏低的是
A.酸式滴定管未用标准醋酸润洗就直接注入标准醋酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取醋酸体积时,开始仰视读数,滴定结束后俯视读数
(3)某学生根据3次实验分别记录有关数据如表:
滴定次数 | 待测氢氧化钠溶液 的体积(ml) | 0.100mol/L醋酸的体积 | |
| 滴定前的刻度(ml) | 滴定后的刻度(ml) | ||
| 第一次 | 25.00 | 0.00 | 24.98 |
| 第二次 | 25.00 | 1.56 | 27.86 |
| 第三次 | 25.00 | 0.22 | 25.24 |
(4)如图2为上述25mL NaOH溶液中逐滴滴加CH3COOH溶液过程中溶液pH的变化曲线.请回答:
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?
②在AB区间内,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)的大小关系是
A.c(OH-)一定大于c(CH3COO-) B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)可能等于c(CH3COO-)
③在D点时,溶液中c(CH3COO-)+c(CH3COOH)
考点:中和滴定,酸碱混合时的定性判断及有关ph的计算
专题:实验题,电离平衡与溶液的pH专题
分析:(1)用标准醋酸滴定待测的氢氧化钠溶液时,锥形瓶中盛放氢氧化钠溶液,滴定管中盛放醋酸溶液,指示剂应该选用酚酞;滴定时,眼睛要注视锥形瓶内溶液的颜色变化;滴定终点时红色变为浅红色,且在半分钟内溶液颜色不改变;
(2)根据c(待测)=
分析不当操作对V(标准)的影响,此判断浓度的误差;
(3)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(醋酸),接着根据醋酸和NaOH反应的关系式:NaOH~CH3COOH,求出C(NaOH);
(4)①NaOH与CH3COOH恰好完全反应,生成醋酸钠,醋酸钠为强碱弱酸盐,水解后溶液显碱性,pH>7;
②在AB区间内,包括CH3COOH和NaOH恰好完全反应以及CH3COOH不足,氢氧化钠过量溶液显碱性两种可能性;
③在D点时,NaOH和CH3COOH反应后剩余CH3COOH,溶液组成为等浓度的CH3COOH和CH3COONa的混合物.
(2)根据c(待测)=
| c(标准)V(标准) |
| V(待测) |
(3)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(醋酸),接着根据醋酸和NaOH反应的关系式:NaOH~CH3COOH,求出C(NaOH);
(4)①NaOH与CH3COOH恰好完全反应,生成醋酸钠,醋酸钠为强碱弱酸盐,水解后溶液显碱性,pH>7;
②在AB区间内,包括CH3COOH和NaOH恰好完全反应以及CH3COOH不足,氢氧化钠过量溶液显碱性两种可能性;
③在D点时,NaOH和CH3COOH反应后剩余CH3COOH,溶液组成为等浓度的CH3COOH和CH3COONa的混合物.
解答:
解:(1)根据题干信息,锥形瓶中应该盛放氢氧化钠溶液,滴定管中盛放醋酸,二者恰好反应时溶液显示碱性,应该使用酚酞作为指示剂,所以C正确;酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化,滴定终点时溶液颜色由红色变为无色,且半分钟内不褪色;
故答案为:C;注视锥形瓶内溶液颜色变化;红色变为浅红色,且在半分钟内溶液颜色不改变;
(2)A.酸式滴定管未用标准醋酸润洗就直接注入标准醋酸,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=
可知,测定c(NaOH)偏大,故A不符合;
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
可知,测定c(NaOH)无影响,故B不符合;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
可知,测定c(NaOH)偏大,故C不符合;
D.读取醋酸体积时,开始仰视读数,滴定结束后俯视读数,造成V(标准)偏小,根据c(待测)=
可知,定c(NaOH)偏低,故D符合;
故选D;
(3)3次实验消耗醋酸的体积分别为:24.98mL、26.30mL、25.02mL,舍去第二组数据,则平均消耗V(醋酸)=25.00mL,
NaOH~CH3COOH,
25.00×C(NaOH) 25.00mL×0.100mol/L
则c(NaOH)=0.10mol/L
故答案为:0.10mol/L;
(4)①NaOH与CH3COOH恰好完全反应:NaOH+CH3COOH=CH3COONa+H20,生成的醋酸钠为强碱弱酸盐,溶液显碱性,pH>7,介于AB之间;
故答案为:否;AB;
②在AB区间内,c(OH-)>c(H-),说明溶液显碱性,当NaOH和CH3COOH恰好反应时,显碱性,此时生成的溶液可能为醋酸钠,c(OH-)小于c(CH3COO-);当NaOH和CH3COOH反应后剩余NaOH,溶液仍然显碱性,此时若剩余的NaOH量很大,则c(OH-)大于c(CH3COO-),也有可能剩余的NaOH和CH3COONa中CH3COO-水解之后剩余的CH3COO-的浓度相等;
故选:C;
③在D点时,反应后CH3COOH剩余,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物,根据物料守恒,此时:c(CH3COO-)+c(CH3COOH)=2c(Na+);
故选:=.
故答案为:C;注视锥形瓶内溶液颜色变化;红色变为浅红色,且在半分钟内溶液颜色不改变;
(2)A.酸式滴定管未用标准醋酸润洗就直接注入标准醋酸,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=
| c(标准)V(标准) |
| V(待测) |
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
| c(标准)V(标准) |
| V(待测) |
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
| c(标准)V(标准) |
| V(待测) |
D.读取醋酸体积时,开始仰视读数,滴定结束后俯视读数,造成V(标准)偏小,根据c(待测)=
| c(标准)V(标准) |
| V(待测) |
故选D;
(3)3次实验消耗醋酸的体积分别为:24.98mL、26.30mL、25.02mL,舍去第二组数据,则平均消耗V(醋酸)=25.00mL,
NaOH~CH3COOH,
25.00×C(NaOH) 25.00mL×0.100mol/L
则c(NaOH)=0.10mol/L
故答案为:0.10mol/L;
(4)①NaOH与CH3COOH恰好完全反应:NaOH+CH3COOH=CH3COONa+H20,生成的醋酸钠为强碱弱酸盐,溶液显碱性,pH>7,介于AB之间;
故答案为:否;AB;
②在AB区间内,c(OH-)>c(H-),说明溶液显碱性,当NaOH和CH3COOH恰好反应时,显碱性,此时生成的溶液可能为醋酸钠,c(OH-)小于c(CH3COO-);当NaOH和CH3COOH反应后剩余NaOH,溶液仍然显碱性,此时若剩余的NaOH量很大,则c(OH-)大于c(CH3COO-),也有可能剩余的NaOH和CH3COONa中CH3COO-水解之后剩余的CH3COO-的浓度相等;
故选:C;
③在D点时,反应后CH3COOH剩余,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物,根据物料守恒,此时:c(CH3COO-)+c(CH3COOH)=2c(Na+);
故选:=.
点评:本题主要考查了中和滴定操作、误差分析以及计算,溶液的酸碱性判断、题目难度中等,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列关于气体摩尔体积的叙述中,正确的是( )
| A、1 mol任何气体的体积都约是22.4 L |
| B、标准状况时,氧气的体积约是22.4 L |
| C、1 molH2和1 molH2O在标准状况下体积都约是22.4 L |
| D、1 mol任何气体在标准状况下所占体积都约是22.4 L |
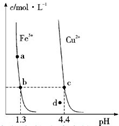 某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )
某温度下,Fe (OH)3(s)、Cu (OH)2 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液 pH,金属阳离子浓度的变化如图所示.据图分析,则下列判断错误的是( )| A、Ksp〔Fe (OH)3〕<Ksp〔Cu (OH)2〕 |
| B、加适量NH4Cl固体可使溶液由a 点变到b点 |
| C、c、d两点代表的溶液中c(H+) 与c(OH-)乘积相等 |
| D、Fe (OH)3、Cu (OH)2分别在b、c两点代表的溶液中达到饱和 |
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: