题目内容
下列关于气体摩尔体积的叙述中,正确的是( )
| A、1 mol任何气体的体积都约是22.4 L |
| B、标准状况时,氧气的体积约是22.4 L |
| C、1 molH2和1 molH2O在标准状况下体积都约是22.4 L |
| D、1 mol任何气体在标准状况下所占体积都约是22.4 L |
考点:气体摩尔体积
专题:化学用语专题
分析:气体摩尔体积的概念是标准状况下1mol任何气体的条件约为22.4L,据此分析选项.
解答:
解:A、温度压强不知,气体摩尔体积不一定为22.4L,故A错误;
B、气体摩尔体积单位为L/mol,标准状况时,氧气的气体摩尔体积约是22.4 L/mol,故B错误;
C、水标准状况不是气体,故C错误;
D、在标准状况下,1 mol任何气体所占体积都约是22.4 L,故D正确;
故选D.
B、气体摩尔体积单位为L/mol,标准状况时,氧气的气体摩尔体积约是22.4 L/mol,故B错误;
C、水标准状况不是气体,故C错误;
D、在标准状况下,1 mol任何气体所占体积都约是22.4 L,故D正确;
故选D.
点评:本题考查了气体摩尔体积的概念分析和条件应用判断,掌握概念实质和条件应用为解题关键,题目较简单.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
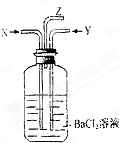 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列说法正确的是( )| A、洗气瓶中产生的沉淀是BaCO3 |
| B、在Z导管出来的气体中无CO2 |
| C、洗气瓶中产生的沉淀是BaSO3 |
| D、在Z导管口有红棕色气体出现 |
加热NH4HCO3固体,使产生的气体依次通过盛有过量Na2O2的干燥管、浓H2SO4的洗气瓶,最后得到的气体是 ( )
| A、O2 |
| B、NH3 |
| C、CO2 |
| D、CO2和O2 |
 科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°.下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的 N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°.下列有关N(NO2)3的说法正确的是( )| A、分子中N、O原子间形成的共价键是非极性键 |
| B、分子中四个氮原子共平面 |
| C、该物质既有氧化性又有还原性 |
| D、分子中四个氮原子围成一个空间正四面体 |
将15%的NaOH溶液蒸发掉100g水后得到125ml质量分数为30%的NaOH溶液,则此时溶液的物质的量浓度为( )
| A、6 mol?L-1 |
| B、6.25 mol?L-1 |
| C、6.75 mol?L-1 |
| D、7 mol?L-1 |
下列离子方程式书写正确的是( )
| A、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO2↑+H2O |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、氢氧化钠溶液吸收过量的二氧化碳:2OH-+CO2=CO32-+H2O |
| D、铝与氢氧化钠溶液反应:Al+OH-+H2O=AlO2-+H2↑ |
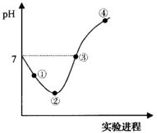 常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol?L-1的氢氧化钠溶液,整个过程中pH( )
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol?L-1的氢氧化钠溶液,整个过程中pH( )| A、①点所示溶液中:c(H+)=c(Cl-)+c(ClO-) |
| B、②点所示溶液中:c(H+)>c(Cl-)>c(ClO-)>c(HClO) |
| C、③点所示溶液中:c(Na+)=c(HClO)+2c(ClO-) |
| D、④点所示溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |