题目内容
一定量的CuS和Cu2S的混合物投人足量的硝酸中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量的NaOH溶液,产生蓝色沉淀,过滤,洗涤,灼烧,得到24.0g CuO.若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
| A、18.0L |
| B、27.0L |
| C、31.4L |
| D、33.6L |
考点:有关混合物反应的计算
专题:计算题
分析:利用极限法解答,假设混合物全是CuS,或混合物全是Cu2S,根据n=
计算n(CuO),根据电子转移守恒计算n(CuS)、n(Cu2S),再根据电子转移数目守恒计算n(NO)、n(NO2),根据V=nVm计算气体体积,实际气体介于二者之间.
| m |
| M |
解答:
解:若混合物全是CuS,其物质的量n(CuS)=n(CuO)=
=0.3mol,转移电子物质的量=0.3×(6+2)=2.4mol.NO和NO2的体积相等,设NO的物质的量为x、NO2的物质的量为x,根据电子转移守恒,则3x+x=2.4,解得x=0.6,故气体体积V=0.6mol×2×22.4L/mol=26.88L;
若混合物全是Cu2S,其物质的量n(Cu2S)=
n(CuO)=
×0.3mol=0.15mol,转移电子物质的量0.15×10=1.5mol,设NO为xmol、NO2为xmol,根据电子转移守恒,3x+x=1.5,解得x=0.375,气体体积0.375mol×2×22.4L/mol=16.8L,
实际气体介于二者之间,
故选A.
| 24g |
| 80g/mol |
若混合物全是Cu2S,其物质的量n(Cu2S)=
| 1 |
| 2 |
| 1 |
| 2 |
实际气体介于二者之间,
故选A.
点评:本题考查氧化还原反应计算,难度中等,注意守恒思想与极限法的利用,是对学生综合能力的考查.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
下列判断正确的是( )
| A、根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B、根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C、晶体中一定存在化学键 |
| D、正四面体分子中键角可能是109°28′或60° |
现有MgCl2、AlCl3、CuCl2、FeCl3、NH4Cl五种溶液,只用一种试剂把它们区别开来,这种试剂是( )
| A、氨水 |
| B、AgNO3 |
| C、NaOH |
| D、H2SO4 |
下列说法正确的是( )
| A、碘是人体必需的微量元素,所以要多吃富含I2的食物 |
| B、金属钠、钾、锂保存在煤油中 |
| C、碳酸钠溶液用带磨口玻璃塞的普通试剂瓶贮存 |
| D、量筒、容量瓶、滴定管上均标有温度 |

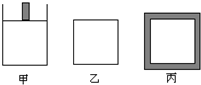 800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行.
800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行. 某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.
某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.