题目内容
下列说法正确的是( )
| A、碘是人体必需的微量元素,所以要多吃富含I2的食物 |
| B、金属钠、钾、锂保存在煤油中 |
| C、碳酸钠溶液用带磨口玻璃塞的普通试剂瓶贮存 |
| D、量筒、容量瓶、滴定管上均标有温度 |
考点:微量元素对人体健康的重要作用,计量仪器及使用方法,化学试剂的存放
专题:元素及其化合物,化学实验常用仪器
分析:A.人体补碘,不是碘单质,是元素,碘单质对人有害;
B.锂密度密度小于煤油,锂会浮在煤油表面;
C.玻璃中的二氧化硅能和碱溶液发生反应,生成具有粘性的硅酸钠,将玻璃塞和玻璃瓶粘到一块;
D.溶液的体积与温度有关.
B.锂密度密度小于煤油,锂会浮在煤油表面;
C.玻璃中的二氧化硅能和碱溶液发生反应,生成具有粘性的硅酸钠,将玻璃塞和玻璃瓶粘到一块;
D.溶液的体积与温度有关.
解答:
解:A.碘单质对人有害,补碘指的是碘元素,如碘酸钾,不是碘单质,故A错误;
B.锂的密度小于煤油,放入煤油中锂会浮在煤油表面,所以金属锂不能保存在煤油中,故B错误;
C.碳酸钠溶液水解呈碱性,玻璃中的二氧化硅能和碱溶液发生反应,生成具有粘性的硅酸钠,将玻璃塞和玻璃瓶粘到一块,故C错误;
D.溶液的体积与温度有关,量筒、容量瓶、滴定管都与体积有关,与温度有关,故D正确.
故选D.
B.锂的密度小于煤油,放入煤油中锂会浮在煤油表面,所以金属锂不能保存在煤油中,故B错误;
C.碳酸钠溶液水解呈碱性,玻璃中的二氧化硅能和碱溶液发生反应,生成具有粘性的硅酸钠,将玻璃塞和玻璃瓶粘到一块,故C错误;
D.溶液的体积与温度有关,量筒、容量瓶、滴定管都与体积有关,与温度有关,故D正确.
故选D.
点评:本题考查常见实验仪器的结构与使用方法、物质的保存等知识,难度不大,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
一定量的CuS和Cu2S的混合物投人足量的硝酸中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量的NaOH溶液,产生蓝色沉淀,过滤,洗涤,灼烧,得到24.0g CuO.若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
| A、18.0L |
| B、27.0L |
| C、31.4L |
| D、33.6L |
下列物质可用水鉴别的是( )
| A、苯、乙醇 |
| B、NH3、HCl |
| C、AgCl、BaSO4 |
| D、NH4Cl、NaCl |
两种气态烃以任意比例混合,在150℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,下列各组混合烃中不符合此条件的是( )
| A、CH4 C2H4 |
| B、CH4 C3H6 |
| C、C2H4 C3H4 |
| D、CH4 C3H4 |
将质量为W1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,溶液澄清,共收集到标准状况下的气体V1 L.向溶液中逐滴加入浓度为a mol/L的盐酸,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加盐酸体积为V2 L,将溶液在HCl气氛中小心蒸干得固体W2 g.下列所列关系式中正确的是( )
| A、35.5aV2=(W2-W1) | ||
B、n(Na)+3n(Al)=
| ||
C、n(Al)>
| ||
D、aV2=
|
我国自主研制可治疗H7N9禽流感新药帕拉米韦,结构如图.下列有关说法正确的是( )

| A、该有机物的分子式是C15H27O4N4 |
| B、该分子中含有氨基、羧基、羟基、醛基等官能团 |
| C、该分子不仅具有两性,还能发生水解反应和酯化反应 |
| D、该分子中含有5个手性碳原子 |

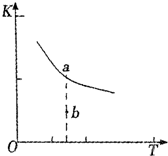 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.