题目内容
1.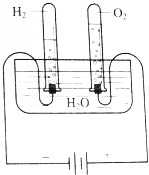 (1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成O2、H2的质量,根据O2、H2的摩尔质量,计算物质的量,并通过下表进行比较.
| 质量g | 物质的量 | H2 和O2物质的量的比 | |
| H2 | |||
| O2 |
分析 (1)方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$=2H2↑+O2↑,H2和O2体积的比值等于物质的量之比;
(2)结合反应的方程式计算
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
36 4 32
1.8g 0.2 g 1.6 g
n(H2)=$\frac{0.2g}{2g/mol}$=0.1mol,n(O2)=$\frac{1.6g}{32g/mol}$=0.05mol,
H2 和O2物质的量的比2:1,
解答 解:(1)方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$=2H2↑+O2↑,H2和O2体积的比值等于物质的量之比,为2:1,
答:生成的O2和H2体积的比各约为2:1;
(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
36 4 32
1.8g 0.2 g 1.6 g
n(H2)=$\frac{0.2g}{2g/mol}$=0.1mol,n(O2)=$\frac{1.6g}{32g/mol}$=0.05mol,
H2 和O2物质的量的比2:1,
根据该实验的观察与推算初步得到关于气体体积规律的一个结论是:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子;同温同压下,气体的体积之比等于其物质的量之比,也等于其分子数之比,在相同温度和压强下.1molO2和H2的体积相同,
故答案为:
| 质量g | 物质的量mol | H2 和O2物质的量的比 | |
| H2 | 0.2 | 0.1 | 2:1 |
| O2 | 1.6 | 0.05 |
点评 本题综合考查阿伏伽德罗定律的测定,侧重于学生的分析能力、实验能力和计算能力的考查,为高频考点,注意数据的对比和信息的整合,题目难度中等.

| A. | MgCl2 | B. | Ca(OH)2 | C. | H2O | D. | N2 |
| A. | BaCl2 | B. | MgCl2 | C. | KCl | D. | FeCl3 |
| A. | 11种 | B. | 13种 | C. | 14种 | D. | 16种 |
| A. | 与电源正极相连的电极上发生还原反应 | |
| B. | 与电源负极相连的电极称为电解池的阴极 | |
| C. | 电解熔融氯化钠时,阳极上析出Cl2 | |
| D. | 电解是电能转化为化学能的过程 |
| A. | 100mL | B. | 101mL | C. | 119mL | D. | 120mL |
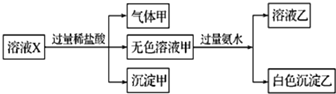
| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸镁的混合物 | |
| C. | K+、AlO2-和SiO32-一定存在于溶液X中 | |
| D. | 仅凭以上实验不能确定SO42-是否存在于溶液X中 |