题目内容
9.处于同主族的相邻两种非金属元素A和B,A的最高价氧化物的水化物的酸性比B弱,A处于B的下边(上或下);B的原子半径比A小;若B的原子序数为x且核外电子层数为3,且则A的原子序数为x+18(用含x的式子表示).分析 处于同主族的相邻两种非金属元素A和B,A的最高价氧化物的水化物的酸性比B弱,则非金属性A<B,A在B的下方,A的原子半径大,B的核外电子层数为3,B位于第三周期,A位于第四周期,在周期表的右侧,原子序数差为第四周期的元素种类数,以此来解答.
解答 解:处于同主族的相邻两种非金属元素A和B,A的最高价氧化物的水化物的酸性比B弱,则非金属性A<B,A处于B的下边;B的原子半径比A小;若B的原子序数为x且核外电子层数为3,且则A的原子序数为x+18,
故答案为:下;小;x+18.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、原子序数关系为解答的关键,侧重分析与应用能力的考查,注意非金属位于周期表的右侧,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列有关仪器使用方法或实验操作正确的是( )
| A. | 洗净的锥形瓶和容量瓶可以放进烘箱中烘干 | |
| B. | 酸式滴定管装标准溶液前,必须先用该溶液润洗 | |
| C. | 酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差 | |
| D. | 所有玻璃仪器加热时均需垫石棉网 |
20.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4L H2O中含有的分子数为NA | |
| B. | 28g N2中含有的分子数为NA | |
| C. | 1mol Mg与足量稀盐酸反应转移的电子数为NA | |
| D. | 1L 1mol•L-1 Na2 CO3溶液中含有的钠离子数为NA |
17.下列物质性质与应用对应关系正确的是( )
| A. | 氧化铝熔点高,可用于制作耐火材料 | |
| B. | 氢氧化铝难溶于水,可用于制胃酸中和剂 | |
| C. | Na2O2具有强氧化性,可用作自来水的消毒剂 | |
| D. | 氧化铁能与酸反应,可用于制作红色涂料 |
4.关于二氧化硫的下列说法中,不正确的是( )
| A. | SO2是硫及其某些硫化物在空气中燃烧的产物 | |
| B. | SO2具有漂白作用,也有防腐作用 | |
| C. | SO2是硫酸的酸酐,称为硫酐 | |
| D. | SO2是一种大气污染物 |
14.一定温度下,可逆反应H2(g)+I2(g)?2HI(g)在容积一定的密闭容器中进行,下列各项中能说明反应已经达到平衡的是( )
| A. | 容器中的压强不变 | B. | 混合物的平均相对分子质量不变 | ||
| C. | 各组分的浓度不变 | D. | 混合气体的密度不变 |
1.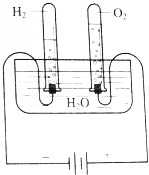 (1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成O2、H2的质量,根据O2、H2的摩尔质量,计算物质的量,并通过下表进行比较.
根据该实验的观察与推算能否初步得出下列结论:在相同温度和压强下.1molO2和H2的体积相同.
 (1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?
(1)根据图所示的电解水原理进行实验,观察不同时间试管内的气体体积的变化.生成的O2和H2体积的比各约为多少?(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成O2、H2的质量,根据O2、H2的摩尔质量,计算物质的量,并通过下表进行比较.
| 质量g | 物质的量 | H2 和O2物质的量的比 | |
| H2 | |||
| O2 |
18.下列说法正确的是( )
| A. | 糖类在一定条件下可以水解生成乙醇和二氧化碳 | |
| B. | 检验淀粉在稀硫酸催化条件下水解产物的方法:取适量水解液于试管中,加入少量新制Cu(OH)2溶液,加热,观察是否出现砖红色沉淀 | |
| C. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 | |
| D. | 蛋白质在紫外线、CuSO4溶液、福尔马林作用下均会发生变性 |
2.某同学在配制一定物质的量浓度的NaCl溶液时,有下列不当操作:
①称量时天平未达平衡(左高右低)
②定容时,眼睛俯视刻度线
这两处不当操作对所得溶液浓度的影响是( )
①称量时天平未达平衡(左高右低)
②定容时,眼睛俯视刻度线
这两处不当操作对所得溶液浓度的影响是( )
| A. | 都导致浓度偏大 | B. | ①导致浓度偏小,②导致浓度偏大 | ||
| C. | 都导致浓度偏小 | D. | ①导致浓度偏大,②导致浓度偏小 |