题目内容
16.有a、b两个密闭容器,已知a容器的容积不变,b容器中的活塞可以上下移动,以保持内外压强相等.在相同条件下将3molA,1molB分别同时混合于a、b两容器中,发生反应3A(g)+B(g)?2C(g)+D(g).回答下列问题:(1)达平衡时,a中A、C的浓度分别M mol/L和N mol/L,b中A、C的浓度分别为m mol/L和n mol/L,则M< m;(填“>”,“<”或无法比较)
(2)若将2molC和2molD充入a中,保持温度不变,平衡时C的浓度为Ymol/L,则Y和N之间的关系为
Y< N;(填“>”,“<”或无法比较)
(3)若将4molC和2molD充入a中,保持温度不变,平衡时A的浓度为W mol/L,则W与M的关系是C
A、W=2M B、W<M C、M<W<2M D、W>2M
(4)保持温度不变,按下列比例分别充入a,b两容器中,达到平衡后a中C的浓度仍为N mol/L的是④⑤,b中C的浓度仍为n mol/L的是①④⑤.
①6molA+2molB ②3molA+2molC ③2molC+1molB+1molD
④2molC+1molD ⑤1.5molA+0.5molB+1molC+0.5molD.
分析 (1)a保持容积不变,为等容变化,b保持内外压强相等,为等压变化,发生反应3A(g)+B(g)?2C(g)+D(g)是气体物质的量减少的反应,故b相当于在a平衡的基础上加压,平衡右移,平衡移动不能消除A的浓度增大,到达新平衡时的浓度高于原平衡,据此解答;
(2)将2 mol C和2 mol D充入a中相当于开始充入3 mol A+1 mol B,平衡时再充入1mol的D,平衡向消耗C的方向移动,所以C的浓度减少;
(3)若将4molC和2molD充入a中,相当于开始充入6 mol A+2 mol B,压强增大,平衡向右移动,反应物转化率增大,参加反应的A的物质的量大于原平衡的2倍,平衡移动不能消除A的浓度增大,到达新平衡时的浓度高于原平衡;
(4)要想达到平衡后a中C的浓度仍为N mol•L-1,与原体系是等效平衡,等温等容的条件下,相同物质的投料量相等;等温等压的条件下,相同物质的投料量相等.
解答 解:(1)a保持容积不变,为等容变化,b保持内外压强相等,为等压变化,发生反应3A(g)+B(g)?2C(g)+D(g)是气体物质的量减少的反应,故b相当于在a平衡的基础上加压,平衡右移,平衡移动不能消除A的浓度增大,到达新平衡时的浓度高于原平衡,故b中平衡时A的浓度大于a中A的平衡浓度,即M<m,故答案为:<;
(2)将2 mol C和2 mol D充入a中相当于开始充入3 mol A+1 mol B,平衡时再充入1mol的D,平衡向消耗C的方向移动,所以C的浓度减少,所以小于N mol•L-1,故答案为:<;
(3)若将4molC和2molD充入a中,相当于开始充入6 mol A+2 mol B,压强增大,平衡向右移动,反应物转化率增大,参加反应的A的物质的量大于原平衡的2倍,平衡时A的浓度小于原平衡的2倍,平衡移动不能消除A的浓度增大,到达新平衡时的浓度高于原平衡,故M<R<2M,
故选:C;
(4)保持温度不变,按下列比例分别充入a、b两容器中,达到平衡后a中C的浓度仍为N mol•L-1,一边倒转化为同一物质,物质的量相同④2molC+1molD ⑤1.5molA+0.5molB+1molC+0.5molD相当于3mol A、1mol B;要想b中C的浓度仍为n mol•L-1,转化为相同物质的物质的量成比例,①6molA+2molB、④2molC+1molD、⑤1.5molA+0.5molB+1molC+0.5molD转化为A与B的物质的量之比3:1,故选:④⑤;①④⑤.
点评 本题考查化学平衡移动与计算,难度中等,注意利用等效思想设计平衡建立的途径,(1)中A的浓度比较为易错点,学生容易根据平衡移动分析判断a中浓度大,忽略体积的减小,注意根据平衡移动原理或平衡常数理解.

| A. | 是否是大量分子或离子的集合体 | B. | 是否均一、透明、稳定 | ||
| C. | 是否能透过滤纸或半透膜 | D. | 分散质微粒直径大小 |
( )
| A. | 该溶液中所含的离子是:Fe2+?Na+?SO42-?NO3-? | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 若向该溶液中加入足量的NaOH 溶液,充分反应后,过滤?洗涤?灼烧,最终所得固体的质量为72g |
| A. | 原子半径逐渐减小 | B. | 电子层数逐渐增多 | ||
| C. | 最高正化合价逐渐升高 | D. | 元素的非金属性逐渐增强 |
| A. | 元素原子的核外电子排布呈周期性变化 | |
| B. | 元素的原子序数呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素的金属性、非金属性呈周期性变化 |
| A. | KF | B. | MgO | C. | H2SO4 | D. | HD |
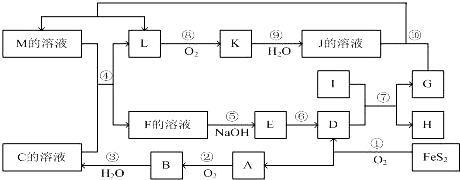
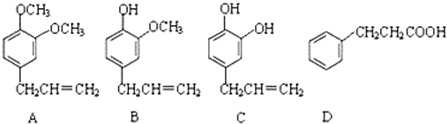
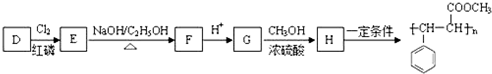
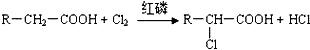
 ;
; .
.