题目内容
5.元素的性质随着元素原子序数的递增而呈周期性变化的根本原因是( )| A. | 元素原子的核外电子排布呈周期性变化 | |
| B. | 元素的原子序数呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素的金属性、非金属性呈周期性变化 |
分析 元素原子的核外电子排布的周期性变化导致元素性质(金属性和非金属性,原子半径,化合价等)的周期性变化,据此进行解答.
解答 解:结构决定性质,即原子的核外电子排布尤其是最外层电子排布决定了元素的性质,故A正确,
故选A.
点评 本题要理解元素周期律的实质,题目难度不大,明确元素周期律的实质为解答关键,注意元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.如用12C质量的$\frac{1}{24}$作为相对原子质量的定义标准,并以0.024kg12C中含有的碳原子数作为阿伏加德罗常数(NA),其他基本物理量的定义方法不变.则采用新的标准时,下列说法正确的是( )
| A. | 2gH2在标态下所占的体积为22.4L | |
| B. | 2.3gNa作还原剂时可失去0.1NA个电子 | |
| C. | 2molNaOH与NA个NA个H2SO4分子恰好中和 | |
| D. | 1molZn与足量的稀硫酸反应时共获得2gH2 |
20.下列数字为几种元素的原子序数,其中位于周期表第三周期的是( )
| A. | 1 | B. | 7 | C. | 8 | D. | 12 |
17.含有下列离子的溶液中,加入氢氧化钠溶液后,离子浓度迅速减少的是( )
| A. | SO42- | B. | SO32- | C. | Cl- | D. | NH4+ |
14.下列表示正确的是( )
| A. | Cl-离子的结构示意图: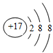 | B. | 乙炔的结构式:CH≡CH | ||
| C. | CH4的球棍模型: | D. | CO2的电子式: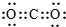 |