题目内容
18.下列有关电解质溶液的描述正确的是( )| A. | 某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | |
| B. | 25℃时,PH=1的醋酸溶液中含有H+的数目小于0.1NA | |
| C. | 在NaHS溶液中滴入CuCl2溶液产生黑色沉淀,HS-水解程度增,pH增大 | |
| D. | 3种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小是①>②>③ |
分析 A、常温下,显酸性的物质有酸、强酸的酸式盐、强酸弱碱盐,据此分析;
B、由溶液的体积不知,所以无法确定氢离子的物质的量;
C、在NaHS溶液中存在HS-?H++S2-,加入CuCl2溶液铜离子与硫离子结合生成硫化铜,导致硫离子浓度减少,促进电离;
D、醋酸钠和碳酸氢钠水解呈碱性,但如果两种弱酸根离子对应的酸越弱,相同的PH的两溶液,所需盐的浓度越小,而氢氧化钠是强碱,所以氢氧化钠的浓度最小.
解答 解:A、常温下,显酸性的物质有酸,如硫酸;强酸的酸式盐,如硫酸氢钠;强酸弱碱盐,如氯化铵;所以25℃时,某物质的溶液pH<7,则该物质一定是酸、强酸的酸式盐、强酸弱碱盐,还与温度有关,如果100℃时水的PH=6<7,故A错误;
B、由溶液的体积不知,所以无法确定氢离子的物质的量,所以氢离子的数目不确定,故B错误;
C、在NaHS溶液中存在HS-?H++S2-,加入CuCl2溶液铜离子与硫离子结合生成硫化铜,导致硫离子浓度减少,促进电离,氢离子的浓度增大,溶液的PH减小,故C错误;D、醋酸钠和碳酸氢钠水解呈碱性,但如果两种弱酸根离子对应的酸越弱,相同的PH的两溶液,所需盐的浓度越小,因为醋酸的酸性强于碳酸,所以pH相同的碳酸氢钠的浓度小醋酸钠的浓度,而氢氧化钠是强碱,所以氢氧化钠的浓度最小,综上所述,c(Na+)的大小是①>②>③,故D正确;
故选D.
点评 本题考查了弱电解质的电离和PH的相关的知识,题目难度中等,注意氢离子的浓度相同时酸根离子越弱对应盐的浓度越小.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
5.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 7.8gNa2O2和Na2S混合物中含有的阴离子数目为0.1NA | |
| B. | pH=13的氢氧化钾溶液,含K+数目约为0.1NA | |
| C. | 标准状况下,5.6LO2作为氧化剂时转移的电子数一定为NA | |
| D. | 18gD2O所含电子数目为10NA |
6.在1.01×105Pa、200℃下,将乙烯、乙醇、乙酸乙酯的混合气vL(已换算成标准状况,下同)在足量的氧气中充分燃烧后,恢复至1.01×105Pa、200℃,测得生成nL混合气(CO2与H2O),消耗氧气mL,下列关系正确的是( )
| A. | v>n | B. | m>n | C. | v<m | D. | 不能确定 |
6.下列说法正确的是( )
| A. | 有机物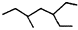 的系统命名为:3-乙基-5-甲基庚烷 的系统命名为:3-乙基-5-甲基庚烷 | |
| B. | 用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质 | |
| C. | 等质量的丁烷、丁烯、1,3-丁二烯分别充分燃烧,所耗氧气的量依次增加 | |
| D. | 糖类、油脂、蛋白质都属于天然有机高分子化合物,都能发生水解反应 |
13.如图中U~Z六种物质在适当条件下能发生如下转化,且反应①、②均为置换反应,下列满足条件的物质组是( )
| 选项 | U | W | Y | X | 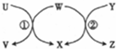 |
| A | Fe | H20 | C | H2 | |
| B | Na | H2O | Na2O2 | NaOH | |
| C | HBr | Cl2 | CH4 | HCl | |
| D | Fe3O4 | Al | NaOH | Al2O3 |
| A. | A | B. | B | C. | C | D. | D |
3.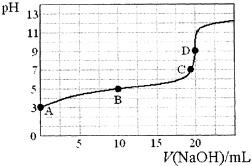 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+ | |
| B. | 常温下,Ka(H3PO2)≈10-5 | |
| C. | 该滴定实验中,用酚酞作指示剂比用甲基橙作指示剂的误差小 | |
| D. | B点溶液中存在关系:c(H+)+c(H3PO2)=c(OH-)+c(H2PO2-) |
10.短周期元素X、Y、Z、W在周期表中位置如图所示.已知Y、W的原子序数之和是Z 的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
| A. | 原子半径:Z>Y>X | B. | 气态氢化物的稳定性:X>Z | ||
| C. | Z、W均能与 Mg 形成离子化合物 | D. | 最高价氧化物的水化物的酸性:Y>W |
7.下列关于N元素在海洋中的循环(如图所示)说法正确的是( )


| A. | 反硝化作用中N元素均被氧化 | |
| B. | N元素所形成的化合物均易溶于水 | |
| C. | N2性质活泼可与多种物质发生反应 | |
| D. | 向海洋排放含NO3-的废水可能影响海洋中N元素循环 |
8.某原子3p轨道上有2个未成对电子,这种元素是( )
| A. | Si | B. | P | C. | S | D. | Cl |