��Ŀ����
3��Mn3O4Ӧ�ù㷺�����������������塢ʯīϩ�缫������ӵ�ص缫�Ȳ��ϣ���̼���̿���Ҫ�ɷ�ΪMnCO3������������+2�ۣ�������+2�ۣ����ܣ�+2�ۣ���̼�������ʣ�Ϊԭ������Mn3O4�Ĺ����������£���ͼ1����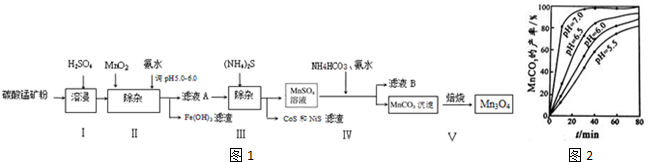
��ش��������⣺
��1��MnS��CoS��NiS�����������У��ܽ��������MnS��
��2��������У�����MnO2��ҪĿ���������������½�Fe2+��������ΪFe3+��
��3��������в����백ˮҲ�ɵõ�̼���̣������백ˮʱ��Ӧ�Ļ�ѧ����ʽ��MnSO4+2NH4HCO3�TMnCO3��+��NH4��2SO4+CO2��+H2O��
��4��25�桢c��Mn2+��=1.05mol/Lʱ��MnCO3�IJ�������ҺpH����Ӧʱ��Ĺ�ϵ��ͼ2��ʾ������ͼ����Ϣ�ó��Ľ�����pH����7.0ʱ��Ӧ������죬��MnCO3�IJ�����ߣ���pHԽ��õ���MnCO3�IJ���Խ�ߣ�����Ҫ��ʱ��Խ�̣�����pH=7ʱ���и��õ�Ч������
��5�����ոߴ��ȵ�MnCO3��s���ɵ�Mn3O4��s����
��֪��25�桢101kpaʱ��
3Mn��s��+2O2��g��=Mn3O4��s����H=-1380kJ/mol
C��s��+O2��g��=CO2��g����H=-394kJ/mol
2Mn��s��+2C��s��+3O2��g��=2MnCO3��s����H=-1790kJ/mol
��MnCO3��s������Mn3O4��s�����Ȼ�ѧ����ʽ��6MnCO3��s��+O2��g��=2Mn3O4��s��+6CO2��g����H=+246kJ/mol��
��6��Mn3O4���Ʊ�����ӵ����������LiMn2O4��ij����ӵ�صĵ�ط�Ӧ�ǣ�
Li1+y-xMn2O4+LixC6=Li1+y Mn2O4+C6�������ĵ缫��Ӧʽ��LixC6-xe-=C6+xLi+�������ĵ缫��Ӧʽ��Li1+y-xMn2O4+xLi++xe-=Li1+yMn2O4��
��6������100t��������Ϊ34.5%��̼���̿��������̣���������н�����Ϊ90%��������м���MnO2�������Ԫ���൱��2610kg MnO2���������������Ԫ�ص���������Ϊ90%���ɵõ�Mn3O420610kg������ʾ��MnCO3��MnO2��Mn3O4����Ħ�������ֱ�Ϊ115��87��229g/mol��
���� ��̼���̿���Ҫ�ɷ�ΪMnCO3������������+2�ۣ�������+2�ۣ����ܣ�+2�ۣ���̼�������ʣ��м������ᣬ��Щ̼���κ�ϡ���ᷴӦ���������Σ�����Һ�м���������̡���ˮ��������Һ��pH�����Խ�������������Ϊ�����ӣ�����pH���Խ�����������������������ҺA�м�����泥����Խ������ӡ��������γ�����������������˺�õ���������Һ������Һ�м���̼����李���ˮ���õ�̼���̳�������ҺB������̼���̹���õ�Mn3O4��
��1������III��IV�ķ�Ӧȷ��MnS��CoS��NiS�������������ܽ���������ʣ�
��2��MnO2���������ԣ���������ԭ�Ե������ӣ�
��3��������в����백ˮҲ�ɵõ�̼���̣������백ˮʱ̼����狀������̷�Ӧ����̼���̳�����
��4������ʱ�䡢��Һ��pH��̼���̲��ʹ�ϵ�������
��5�����ݸ�˹���ɼ��㷴Ӧ�ȣ�
��6����ط�Ӧʽ��ȥ������Ӧʽ����������Ӧʽ��
��7������MnԪ���غ����Mn3O4��������
��� �⣺��̼���̿���Ҫ�ɷ�ΪMnCO3������������+2�ۣ�������+2�ۣ����ܣ�+2�ۣ���̼�������ʣ��м������ᣬ��Щ̼���κ�ϡ���ᷴӦ���������Σ�����Һ�м���������̡���ˮ��������Һ��pH�����Խ�������������Ϊ�����ӣ�����pH���Խ�����������������������ҺA�м�����泥����Խ������ӡ��������γ�����������������˺�õ���������Һ������Һ�м���̼����李���ˮ���õ�̼���̳�������ҺB������̼���̹���õ�Mn3O4��
��1������III��IV�ķ�Ӧȷ��MnS��CoS��NiS�������������ܽ������������MnS���ʴ�Ϊ��MnS��
��2��MnO2���������ԣ���������ԭ�Ե������ӣ�������Һ��pH�Ӷ�����Ԫ�س�ȥ���ʴ�Ϊ�������������½�Fe2+��������ΪFe3+��
��3��������в����백ˮҲ�ɵõ�̼���̣������백ˮʱ̼����狀������̷�Ӧ����̼���̳�������Ӧ����ʽΪMnSO4+2NH4HCO3�TMnCO3��+�� NH4��2SO4+CO2��+H2O���ʴ�Ϊ��MnSO4+2NH4HCO3�TMnCO3��+�� NH4��2SO4+CO2��+H2O��
��4������ͼ֪pH����7.0ʱ��Ӧ������죬��MnCO3�IJ�����ߣ���pHԽ��õ���MnCO3�IJ���Խ�ߣ�����Ҫ��ʱ��Խ�̣�����pH=7ʱ���и��õ�Ч������
�ʴ�Ϊ��pH����7.0ʱ��Ӧ������죬��MnCO3�IJ�����ߣ���pHԽ��õ���MnCO3�IJ���Խ�ߣ�����Ҫ��ʱ��Խ�̣�����pH=7ʱ���и��õ�Ч������
��5����3Mn��s��+2O2��g��=Mn3O4��s����H=-1380kJ/mol
��C��s��+O2��g��=CO2��g����H=-394kJ/mol
��2Mn��s��+2C��s��+3O2��g��=2MnCO3��s����H=-1790kJ/mol
������ʽ2��+6��-3��6MnCO3��s��+O2��g��=2Mn3O4��s��+6CO2��g����H=2��-1380kJ/mol
��+6��-394kJ/mol��-3��-1790kJ/mol��=+246kJ/mol��
�ʴ�Ϊ��6MnCO3��s��+O2��g��=2Mn3O4��s��+6CO2��g����H=+246kJ/mol��
��6����ط�Ӧʽ��ȥ������Ӧʽ����������ӦʽΪLi1+y-xMn2O4+xLi++xe-=Li1+y Mn2O4���ʴ�Ϊ��Li1+y-xMn2O4+xLi++xe-=Li1+y Mn2O4��
��7����Mn3O4������Ϊxkg������MnԪ���غ�ã�1��10000kg��34.5%��$\frac{55}{115}$��90%+2610kg��$\frac{55}{87}$����90%=xkg��$\frac{165}{229}$��x=20610��
�ʴ�Ϊ��20610��
���� ���⿼�����ʷ�����ᴿ��Ϊ��Ƶ���㣬�漰������ԭ��Ӧ��������������˹���ɡ�ԭ���ԭ�������������йؼ����֪ʶ�㣬�ۺ��Խ�ǿ����ȷ������ѧԭ�����������������������ǽⱾ��ؼ�����Ϥ����ͼ�л������������������ķ�Ӧ����Ŀ�Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | ˮ�ĵ�����һ�����ȹ��̣��¶����ߣ�ˮ�����ӻ�KWҲ���� | |
| B�� | ��pH����2����λʱ����Һ��c��H+������20�� | |
| C�� | pH=2.0������Һ��ϡ��10��ʱ��pHΪ3 | |
| D�� | ��Һϡ��ʱ��c��H+�����٣�pH���� |
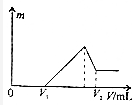 ��0.1mol��þ�������������100mL2mol/LH2SO4��Һ�У�Ȼ���ٵμ�1mol/LNaOH��Һ�����ڵμ�NaOH��Һ�Ĺ����У���������m�����NaOH��Һ�����V�仯��ͼ��ʾ����V2=460mLʱ����ԭ�������þ�����������ǣ�������
��0.1mol��þ�������������100mL2mol/LH2SO4��Һ�У�Ȼ���ٵμ�1mol/LNaOH��Һ�����ڵμ�NaOH��Һ�Ĺ����У���������m�����NaOH��Һ�����V�仯��ͼ��ʾ����V2=460mLʱ����ԭ�������þ�����������ǣ�������| A�� | 1��1 | B�� | 2��3 | C�� | 16��27 | D�� | 8��9 |
| ѡ�� | ʵ����������� | ���ͻ���� |
| A | �����������м���ϡ�����У���ַ�Ӧ����KSCN��Һ����Һ�ʺ�ɫ | ϡ���ὫFe����ΪFe3+ |
| B | AgI�����е���KCl��Һ�������ɻ�ɫ��Ϊ��ɫ | AgI��AgCl���� |
| C | ��������ϡ�����У������� | �������汻�����������γ����ܵ�����Ĥ |
| D | ������Һ�еμ���ˮ�����ְ�ɫ���� | ��������ȡ����Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | 7.2gC5H12���й��ۼ���Ϊ1.6NA | |
| B�� | 14g��ϩ�ͱ�ϩ�Ļ�����к���ԭ�ӵ���ĿΪNA | |
| C�� | ��״���£�224mL������ȼ�պ����ɵ�CO2�ķ�����Ϊ0.06NA | |
| D�� | 1.7g�ǻ���-OH�����еĵ�����ΪNA |
 a��b��c��d������ԭ��������������Ķ�����Ԫ�أ�aԭ�ӵĵ��Ӳ���Ϊn��������������2n2-1������������Ϊ2n+l��b��dͬ���壬���γ�������ѧ�����Ļ����c��b��ɵĻ�������һ�������������ҵ��ͨ�����û������ұ��c���ʣ�eԭ�����ĸ��ܲ㣬��δ�ɶԵ�������ͬ���������ģ��ش��������⣺
a��b��c��d������ԭ��������������Ķ�����Ԫ�أ�aԭ�ӵĵ��Ӳ���Ϊn��������������2n2-1������������Ϊ2n+l��b��dͬ���壬���γ�������ѧ�����Ļ����c��b��ɵĻ�������һ�������������ҵ��ͨ�����û������ұ��c���ʣ�eԭ�����ĸ��ܲ㣬��δ�ɶԵ�������ͬ���������ģ��ش��������⣺