题目内容
14.下列说法正确的是( )| A. | 水的电离是一个吸热过程,温度升高,水的离子积KW也增大 | |
| B. | 当pH减少2个单位时,溶液中c(H+)增大20倍 | |
| C. | pH=2.0的酸溶液,稀释10倍时,pH为3 | |
| D. | 溶液稀释时,c(H+)减少,pH增大 |
分析 A.水的电离是吸热反应,升高温度促进水电离;
B、根据pH=-lgc(H+)来计算;
C、强酸和弱酸的稀释存在不同点,弱酸的稀释会促进电离;
D、酸溶液稀释时,pH增加,但是碱溶液稀释时,pH减小.
解答 解:A.水的电离是吸热反应,升高温度促进水电离,水中氢离子、氢氧根离子浓度都增大,所以离子积常数增大,故A正确;
B、当pH减少2个单位时,溶液中c(H+)增大100倍,故B错误;
C、pH=2.0的强酸溶液,稀释10倍时,pH=3,pH=2.0的弱酸溶液,稀释10倍时,pH<3,故C错误;
D、酸溶液稀释时,酸中c(H+)减少,pH增加,但是碱溶液稀释时,c(H+)增加,pH减小,故D错误.
故选A.
点评 本题考查学生弱电解质的电离以及溶液pH的计算等知识,属于基础知识的考查,难度中等.

练习册系列答案
相关题目
4.欲除去CuSO4•5H2O中的沙子,必要的实验操作为( )
| A. | 溶解 过滤 蒸发结晶 | B. | 加热 溶解 过滤 | ||
| C. | 溶解 过滤 蒸馏 | D. | 溶解 过滤 分液 |
2.下列反应属于氧化还原反应,又属于离子反应和化合反应的是( )
| A. | 硅和氢氧化钠溶液反应 | B. | 二氧化碳通入饱和Na2CO3溶液 | ||
| C. | 镁在二氧化碳中燃烧 | D. | 氯气通入到氯化亚铁溶液中 |
19.下列关于乙烯和聚乙烯的叙述中正确的是( )
| A. | 二者互为同系物 | |
| B. | 聚乙烯是乙烯的缩聚产物 | |
| C. | 二者都能使溴的四氯化碳溶液褪色 | |
| D. | 等质量的乙烯和聚乙烯分别完全燃烧消耗等物质的量的氧气,生成等量的水 |
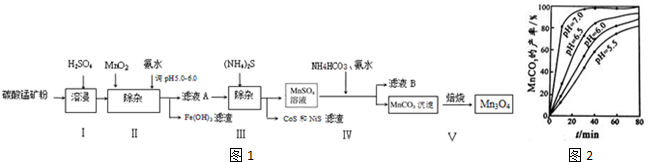
4.高炉炼铁的烟尘中主要含有锌、铁、铜等金属元素.从烟尘中提取硫酸锌,可以变废为宝,减少其对环境的危害.图是用高炉烟尘制取硫酸锌的工业流程.

已知:
①20℃时,0.1mol•L-1的金属离子沉淀时的pH
②过二硫酸铵是一种强氧化剂.
③ZnSO4+4NH3=[Zn(NH3)4]SO4,[Zn(NH3)4]SO4易溶于水.
回答下列问题:
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?(举出1种)升高温度.
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是pH计.
(3)加入MnO2的目的是将Fe2+氧化成Fe3+.
(4)写出还原过程发生的主要反应的离子方程式Zn+Cu2+=Zn2++Cu.
(5)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式MnSO4+(NH4)2S2O8+2H2O=MnO2+(NH4)2SO4+2H2SO4.
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是C
A、锌粉 B、氨水 C、(NH4)2CO3 D、NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值10-1.6mol/L.

已知:
①20℃时,0.1mol•L-1的金属离子沉淀时的pH
| pH | Fe3+ | Zn2+ | Mn2+ | Cu2+ |
| 开始沉淀 | 1.9 | 6.0 | 8.1 | 4.7 |
| 沉淀完全 | 3.7 | 8.0 | 10.1 | 6.7 |
| 沉淀溶解 | 不溶解 | 10.5 | 不溶解 | / |
③ZnSO4+4NH3=[Zn(NH3)4]SO4,[Zn(NH3)4]SO4易溶于水.
回答下列问题:
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?(举出1种)升高温度.
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是pH计.
(3)加入MnO2的目的是将Fe2+氧化成Fe3+.
(4)写出还原过程发生的主要反应的离子方程式Zn+Cu2+=Zn2++Cu.
(5)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式MnSO4+(NH4)2S2O8+2H2O=MnO2+(NH4)2SO4+2H2SO4.
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是C
A、锌粉 B、氨水 C、(NH4)2CO3 D、NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值10-1.6mol/L.
 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
; ;
;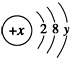 ( y≠0 ).请回答:
( y≠0 ).请回答: