题目内容
2.NaCI是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )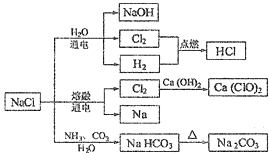
| A. | 常温时,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应可用于制备漂白粉,漂白粉的主要成分是Ca(ClO)2和CaCl2 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
分析 A.根据其阴离子的水解程度判断;
B.根据氯气与氢氧化钙的反应分析;
C.铁能在氯气中燃烧生成棕黄色的烟FeCl3;
D.根据元素的化合价是否变化判断.
解答 解:A.碳酸根的第一步水解(水解后生成碳酸氢根和氢氧根)的平衡常数比碳酸氢根要大许多.碳酸根水解要比碳酸氢根容易得多,所以溶解度较大,且溶解的快,故A错误;
B.石灰乳与Cl2的反应可用于制备漂白粉,2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是Ca(ClO)2和CaCl2,故B正确;
C.铁能在氯气中燃烧生成棕黄色的烟FeCl3,则在一定条件下,Fe与氯气能反应,3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故C错误;
D、氯化钠和水、氨气、二氧化碳的反应以及碳酸氢钠的分解反应都不是氧化还原反应,故D错误.
故选B.
点评 本题考查了盐的溶解性、氧化还原反应、氧化剂还原剂等问题,题目具有一定的综合性,注意根据化合价的变化来分析氧化还原反应,题目难度中等.

练习册系列答案
相关题目
10.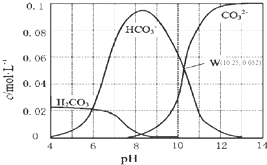 25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
 25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )
25℃时,0.1mol•L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如图所示.下列说法正确的是( )| A. | 在pH=7.0时,溶液中含碳粒子只有CO32-和HCO3- | |
| B. | 0.1 mol•L-1Na2CO3溶液pH=13 | |
| C. | H2CO3的Ka2=1.0×10-10.25 | |
| D. | 向100 mL 0.1 mol•L-1碳酸钠溶液中滴加盐酸至溶液pH=4.0,生成标准状况下CO2气体224 mL |
17.室温时,某溶液中由水电离生成的H+和OH-物质的量浓度的乘积为1×10-24,则在该溶液中一定不能大量共存的离子组是( )
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
7.根据图中包含的信息分析,下列叙述正确的是( )
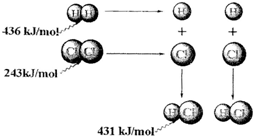

| A. | 氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量 | |
| B. | 436 kJ/mol是指断开1 mol H2中的H-H键需要放出436 kJ的能量 | |
| C. | 431kJ/mol是指生成2 mol HCl中的H-Cl键需要放出431 kJ的能量 | |
| D. | 氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量 |
11.NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 标准状况下,11.2L的乙烷所含的分子数为0.5NA | |
| B. | 0.5mol C3H8分子中含C-H共价键4NA | |
| C. | 11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |

 $\stackrel{H_{2}O}{→}$2RCOOH
$\stackrel{H_{2}O}{→}$2RCOOH 、
、 .
. .
. 、
、 .
.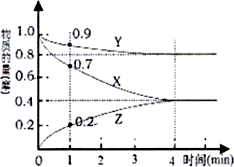 (1)某温度时,在2L的密闭容器在X、Y、Z三种物质的量随时间的变化如图所示.
(1)某温度时,在2L的密闭容器在X、Y、Z三种物质的量随时间的变化如图所示.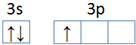 ,第一电离能:镁大于(填“大于”或“小于”)铝.
,第一电离能:镁大于(填“大于”或“小于”)铝.