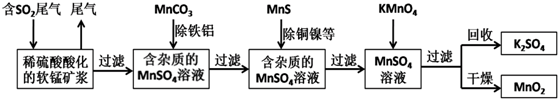
题目内容
14.2015年国产C919大型客机正式下线,标志着我国成为世界上少数几个具有自行研制大型飞机的国家之一,标志着我国航空工业进入了新的发展阶段.(1)飞机的外壳通常采用镁-铝合金材料,铝的价电子排布图为
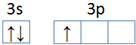 ,第一电离能:镁大于(填“大于”或“小于”)铝.
,第一电离能:镁大于(填“大于”或“小于”)铝.(2)现代飞机为了减轻质量而不减轻外壳承压能力,通常采用复合材料--玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如图所示:
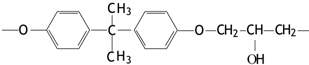
其中碳原子的杂化方式为sp2、sp3,对应个数比为2:1.
分析 (1)Al原子价电子排布式为3s23p1,根据泡利原理、洪特规则画出价电子排布图;Mg元素3s能级为全满稳定状态,第一电离能高于同周期相邻元素的;
(2)分子中碳原子均没有孤对电子,苯环中C原子形成3个σ键、其它碳原子生成4个σ键,杂化轨道数目分别为3、4.
解答 解:(1)Al原子价电子排布式为3s23p1,价电子排布图为,Mg元素3s能级为全满稳定状态,能量较低,Mg的第一电离能大于Al的,
故答案为: ;大于;
;大于;
(2)分子中碳原子均没有孤对电子,苯环中C原子形成3个σ键、其它碳原子生成4个σ键,杂化轨道数目分别为3、4,分别采取sp2、sp3 杂化,二者原子数目之比为12:6=2:1,
故答案为:sp2、sp3;2:1.
点评 本题是对物质结构与性质的考查,涉及核外电子排布图、杂化方式,识记元素周期表中特殊情况,难度中等.

练习册系列答案
相关题目
5.下列物质中属于非电解质的是( )
| A. | 铁 | B. | 蔗糖 | C. | 氯化钠溶液 | D. | 氢氧化铜 |
2.NaCI是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )
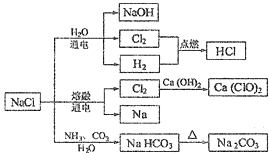

| A. | 常温时,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应可用于制备漂白粉,漂白粉的主要成分是Ca(ClO)2和CaCl2 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应都是氧化还原反应 |
9.下列反应中,属于取代反应的是( )
| A. | 甲烷燃烧 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍做催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气在光照下反应 |
19.下列是四种烷烃分子的结构模型图,其中沸点最高的是( )
| A. |  | B. |  | C. |  | D. |  |
6.下列叙述中,正确的是( )
| A. | 氯气中含有的少量氯化氢,可用氢氧化钠溶液除去 | |
| B. | NaHCO3的热稳定性比Na2CO3强 | |
| C. | 过量铁粉加入CuCl2溶液中,充分反应后溶液中的阳离子主要是Fe3+ | |
| D. | 氨气喷泉实验说明氨气极易溶解于水 |
2.下列说法正确的是( )
| A. | 图(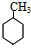 )的一氯代物有4种 )的一氯代物有4种 | |
| B. | 表示甲烷分子或四氯化碳分子的比例模型 | |
| C. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O |