题目内容
5.将0.05mol某烃完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,该烃能使酸性高锰酸钾溶液褪色,若其结构中只含有一个亚甲基,则该烃的结构(不考虑立体异构)最多有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,可知n(CO2)=$\frac{13.2g}{44g/mol}$=0.3mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,由此可确定有机物分子式,该烃能使酸性高锰酸钾溶液褪色,说明含有碳碳双键,结合结构中只含有一个亚甲基确定烃的结构.
解答 解:完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,可知n(CO2)=$\frac{13.2g}{44g/mol}$=0.3mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,
可知有机物中N(C)=$\frac{0.3}{0.05}$=6,N(H)=$\frac{0.3}{0.05}$×2=12,则有机物分子式为C6H12,该烃能使酸性高锰酸钾溶液褪色,说明含有碳碳双键,若其结构中只含有一个亚甲基,可能为CH2=或-CH2-,则可能的结构有CH2=C(CH3)CH(CH3)2、CH2=CHC(CH3)3、CH3C=C(CH3)CH2CH3、CH3C(CH3)=CHCH2CH3,共4种,
故选B.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,注意把握有机物的结构特点,把握同分异构体的判断,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.在强酸性或强碱性溶液中都能大量共存的一组离子是( )
| A. | Ba2+、Fe3+、Br-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
20.下列叙述错误的是( )
| A. | 盛装在敞口玻璃容器中的碘化钾溶液,在空气中久置后,可能会显黄色 | |
| B. | 次氯酸不稳定,见光即分解,可与强碱发生中和反应,则证明次氯酸为弱酸 | |
| C. | 铜粉在氯气中燃烧生成棕色的烟 | |
| D. | 氯水久置后溶液的酸性增强 |
10.邻甲基苯甲酸有多种同分异构体,其中属于酯类且分子结构中有-CH3和苯环的同分异构体有( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
17.1-丙醇的蒸气和空气混合,通过灼热的铜网生成一种新的化合物.下列物质中,和该化合物互为同分异构体的是( )
| A. | CH3CH2CHO | B. | CH3CH2COOH | C. | CH3COCH3 | D. | CH3CH2OCH3 |
14. 某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.
某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.
(1)CO的检测.
①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产生黑色的Pd沉淀,每生成5.3gPd沉淀,反应转移电子数为0.1NA.
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图1所示,这种传感器利用了燃料电池原理.则该电池的负极反应式为CO+H2O-2e-=CO2+2H+.
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
①上述反应T1℃时的平衡常数为K=$\frac{9}{16}$.
②根据上述信息判断,温度T1和T2的关系是(填序号)c.
a.T1>T2 b.T1<T2 c.无法比较
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理为NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O,△<0在氨气足量的情况下,不同$\frac{c(N{O}_{2})}{c(NO)}$、不同温度对脱氨率的影响如图2所示.请回答温度对脱氨率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小;300℃之前,反应未平衡,反应向右进行,脱氮率增大,给出合理的解释300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小.
(4)硫酸厂尾气中的SO2可催化氧化生成SO3,再合成硫酸.在某温度时,向10L的密闭容器中加入4.0molSO2和10.0molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是BC(填序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍.
 某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.
某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.(1)CO的检测.
①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产生黑色的Pd沉淀,每生成5.3gPd沉淀,反应转移电子数为0.1NA.
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图1所示,这种传感器利用了燃料电池原理.则该电池的负极反应式为CO+H2O-2e-=CO2+2H+.
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
 | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②根据上述信息判断,温度T1和T2的关系是(填序号)c.
a.T1>T2 b.T1<T2 c.无法比较
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理为NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O,△<0在氨气足量的情况下,不同$\frac{c(N{O}_{2})}{c(NO)}$、不同温度对脱氨率的影响如图2所示.请回答温度对脱氨率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小;300℃之前,反应未平衡,反应向右进行,脱氮率增大,给出合理的解释300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小.
(4)硫酸厂尾气中的SO2可催化氧化生成SO3,再合成硫酸.在某温度时,向10L的密闭容器中加入4.0molSO2和10.0molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是BC(填序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍.
15.下列试剂能区分苯酚、甲酸、乙酸乙酯、甲醇的是( )
| A. | NaOH溶液 | B. | FeCl3溶液 | C. | 溴水 | D. | 银氨溶液 |
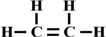 ,空间结构是平面型分子;
,空间结构是平面型分子;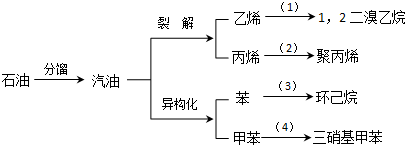
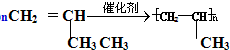 (加成聚合反应)
(加成聚合反应)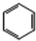 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$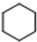 (加成反应)
(加成反应)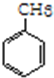 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$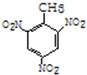 +3H2O(取代反应)
+3H2O(取代反应) .
. .
. (不考虑顺反异构).
(不考虑顺反异构).