题目内容
16.石蜡油在炽热碎瓷片作用下产生乙烯并检验其性质的实验,完成下列问题.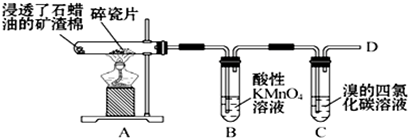
①产生乙烯气体的官能团碳碳双键,产生乙烯气体的结构式
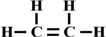 ,空间结构是平面型分子;
,空间结构是平面型分子;②B中反应类型是氧化反应,实验现象是酸性高锰酸钾溶液紫色褪去;
③C中反应类型是加成反应,化学方程式是CH2=CH2+Br-Br→CH2Br-CH2Br;
④在D处点燃前必须进行的操作是检验气体的纯度,实验现象是火焰明亮,伴有黑烟.
分析 ①乙烯分子中含有官能团为碳碳双键,乙烯分子中碳碳原子间是双键,碳原子和氢原子间为单键,分子借故为平面结构;
②乙烯通入氧化剂高锰酸钾溶液中发生氧化反应,溶液紫红色褪去;
③C中通入乙烯和溴单质发生加成反应;
④点燃可燃性气体时应先验纯,乙烯气体燃烧因为含碳量高出现黑烟,出现明亮火焰.
解答 解:①乙烯分子中含有官能团为碳碳双键,乙烯分子中碳碳原子间是双键,碳原子和氢原子间为单键,结构式为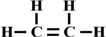 ,分子结构为平面结构,
,分子结构为平面结构,
故答案为:碳碳双键;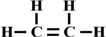 ;平面型分子
;平面型分子
②高锰酸钾具有强氧化性能氧化乙烯生产二氧化碳,所以乙烯通入氧化剂高锰酸钾溶液中发生氧化反应,溶液紫红色褪去,
故答案为:氧化反应;酸性高锰酸钾溶液紫色褪去;
③C中通入乙烯和溴单质发生加成反应,反应的化学方程式为:CH2=CH2+Br-Br→CH2Br-CH2Br,
故答案为:加成反应;CH2=CH2+Br-Br→CH2Br-CH2Br;
④点燃可燃性气体时应先验纯,在D处点燃前必须进行的操作是检验气体的纯度,乙烯气体燃烧因为含碳量高出现黑烟,出现明亮火焰,
故答案为:检验气体的纯度;火焰明亮,伴有黑烟.
点评 本题考查了乙烯的化学性质和结构,题目难度不大,要注意乙烯中含有碳碳双键,有还原性,能使高锰酸钾溶液和溴水褪色,但是反应类型不同.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.硼有两种天然同位素${\;}_{5}^{10}$B、${\;}_{5}^{11}$B,假设硼元素的相对原子质量为10.2,则${\;}_{5}^{11}$B的质量分数为( )
| A. | 20% | B. | 80% | C. | 78.4% | D. | 21.6% |
4.影响化学反应速率的因素很多,下列措施一定能提高反应速率的是( )
| A. | 改变反应物用量 | B. | 增大压强 | C. | 增大体积 | D. | 升高温度 |
11.下列分子中所有原子都满足最外层为8个电子结构的是( )
| A. | BCl3 | B. | NCl3 | C. | H2S | D. | BeCl2 |
8.化合物A、B是中学常见的物质,其阴阳离子可从表中选择
(1)若A的水溶液为无色,B的水溶液呈碱性,A、B的水溶液混合后,只产生不溶于稀硝酸的白色沉淀及能使湿润的红色石蕊试纸变蓝的气体,则
①A中的化学键类型为离子键、共价键(填“离子键”、“共价键”).
②A、B溶液混合后加热呈中性,该反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(请用文字叙述)
Ⅰ仅有I-被氧化成I2使溶液呈黄色.ⅡI-、Fe2+均被氧化使溶液呈黄色.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
④利用上述过程中溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为NO3-+4H++3e-═NO↑+2H2O.
| 阳离子 | K+、Na+、NH4+、Fe2+、Ba2+、Cu2+ |
| 阴离子 | OH-、I-、NO3-、AlO2-、HCO3-、HSO4- |
①A中的化学键类型为离子键、共价键(填“离子键”、“共价键”).
②A、B溶液混合后加热呈中性,该反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(请用文字叙述)
Ⅰ仅有I-被氧化成I2使溶液呈黄色.ⅡI-、Fe2+均被氧化使溶液呈黄色.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
④利用上述过程中溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为NO3-+4H++3e-═NO↑+2H2O.
5.将0.05mol某烃完全燃烧生成的产物依次通过浓硫酸和碱石灰,浓硫酸增重5.4克,碱石灰增重13.2克,该烃能使酸性高锰酸钾溶液褪色,若其结构中只含有一个亚甲基,则该烃的结构(不考虑立体异构)最多有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
6.根据下列实验现象所得出的结论不正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机层呈橙色 | 氧化性:Cl2>KBrO3 |
| B | 向KNO3和KOH混合溶液中加入铝粉并加热,将湿润的红色石蕊试纸放在试管口 | 试纸变为蓝色 | NO3-被还原为NH3 |
| C | 向0.1mol•L-1的Na2CO3溶液中加入两滴酚酞,溶液显浅红色,微热. | 红色加深 | 盐类水解是吸热反应 |
| D | 将0.1mol•L-1的MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1的CuSO4溶液 | 白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
