题目内容
13.(1)请根据以汽油为原料的下列衍变关系,写出相应的化学方程式(有机物写结构简式,不必写反应条件,在括弧中填反应类型).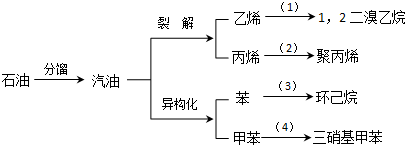
①CH2=CH2+Br2→CH2BrCH2Br(加成反应)
②
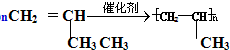 (加成聚合反应)
(加成聚合反应)③
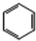 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$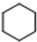 (加成反应)
(加成反应)④
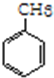 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$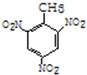 +3H2O(取代反应)
+3H2O(取代反应)(2)下列各组物质,能用酸性高锰酸钾溶液鉴别的是CE.
A.乙烯、乙炔 B.苯、己烷 C.苯、甲苯
D.己烷、环己烷 E.甲烷、乙烯
(3)在戊烷的各种同分异构体中,A不能由某种烯烃和氢气加成获得,其结构简式为
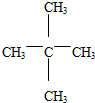 .
.(4)B是苯的同系物,分子式为C9H12,一溴代物只有2种,则B的结构简式为
 .
.(5)氯代烃C的分子式为C4H9Cl,在NaOH乙醇溶液中加热可获得两种沸点不同的烯烃,则C的结构简式为
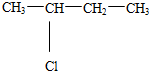 (不考虑顺反异构).
(不考虑顺反异构).
分析 (1)①烯烃与溴单质能发生加成反应得到卤代烃;
②烯烃能发生加聚反应得到聚烯烃;
③苯在催化剂的条件下能和氢气发生加成反应得到环己烷;
④甲苯能与硝酸发生取代反应;
(2)能用酸性高锰酸钾溶液鉴别说明物质遇到高锰酸钾溶液使之褪色可以鉴别;
(3)戊烷存在三种同分异构体,正戊烷、异戊烷、新戊烷,由某种烯烃和氢气加成需要分子中添加双键保证碳原子写出四个共价键,先利用减链法书写同分异构体,然后根据不能由某种烯烃和氢气加成获得判断碳原子上氢原子的种类写出结构简式;
(4)属于芳香烃,则含有1个苯环,剩余3个C,可以是丙基、甲基和乙基或者3个甲基,一溴代物只有2种,说明有2类氢原子,苯环上只有一种H;
(5)C4H10的同分异构体有:CH3CH2CH2CH3、CH3CH(CH3)CH3,利用1个Cl原子替换H原子,分析在NaOH乙醇溶液中加热发生消去反应其符合条件的结构.
解答 解:(1)①乙烯与铝化氢能发生加成反应得到氯乙烷,方程式为:CH2=CH2+Br2→CH2BrCH2Br,反应为加成反应,
故答案为:CH2=CH2+Br2→CH2BrCH2Br;加成反应;
②丙烯能发生加聚反应得到聚丙烯,方程式为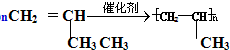 ,反应为加成聚合反应,
,反应为加成聚合反应,
故答案为: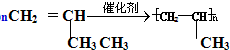 ;加成聚合反应;
;加成聚合反应;
③苯在催化剂的条件下能和氢气发生加成反应得到环己烷,反应的化学方程式为: +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ 反应为加成反应,
反应为加成反应,
故答案为: +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ ; 加成反应;
; 加成反应;
④甲苯能与硝酸发生取代反应, +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$ +3H2O,反应为取代反应,
+3H2O,反应为取代反应,
故答案为: +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$ +3H2O;取代反应;
+3H2O;取代反应;
(2)A.乙烯、乙炔通过高锰酸钾溶液都会被高锰酸钾溶液氧化,溶液紫红色褪去,故A错误;
B.苯、己烷在高锰酸钾溶液中都不能发生氧化反应,溶液不褪色,故B错误;
C.苯、甲苯中甲苯被高锰酸钾溶液氧化,苯不能使高锰酸钾溶液褪色,可以鉴别,故C正确;
D.己烷、环己烷 分子中都是饱和碳原子在高锰酸钾溶液中都不褪色,故D错误;
E.甲烷、乙烯中乙烯通过高锰酸钾溶液会褪色,甲烷不褪色,可以鉴别,故E正确;
故答案为:CE;
(3)戊烷的同分异构体:所有的碳原子在一条链上:CH3-CH2-CH2-CH2-CH3;拿下1个碳原子作为支链: ;拿下2个碳原子作为支链:
;拿下2个碳原子作为支链: ;其中不能由某种烯烃和氢气加成获得,说明有碳上无氢原子即只有一种氢原子,为
;其中不能由某种烯烃和氢气加成获得,说明有碳上无氢原子即只有一种氢原子,为 ,
,
故答案为: ;
;
(4)B是苯的同系物,分子式为C9H12,含有1个苯环,剩余3个C,可以是丙基、甲基和乙基或者3个甲基,一溴代物只有2种,说明有2类氢原子,苯环上只有一种H,则为间三甲苯,其结构简式为 ,
,
故答案为: ;
;
(5)C4H10的同分异构体有:CH3CH2CH2CH3、CH3CH(CH3)CH3,CH3CH2CH2CH3的一氯取代产物有两种:CH3CH2CH2CH2Cl、CH3CH(Cl)CH2CH3,CH3CH(CH3)CH3的一氯取代产物也有两种: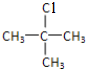 和(CH3)2CHCH2Cl,CH3CH2CH2CH2Cl、
和(CH3)2CHCH2Cl,CH3CH2CH2CH2Cl、 和(CH3)2CHCH2Cl的消去产物都只有一种,所以只有
和(CH3)2CHCH2Cl的消去产物都只有一种,所以只有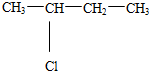 符合;
符合;
故答案为: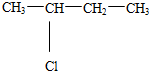 .
.
点评 本题考查有机物结构简式的确定、烯的性质、有机物的性质和方程式的书写知识、有机物的鉴别,侧重常见有机物性质的考查等,题目难度中等,注意同分异构体个数的判断、注意苯环上取代基位置的确定是解决本题的关键.

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案| A. | 改变反应物用量 | B. | 增大压强 | C. | 增大体积 | D. | 升高温度 |
| 阳离子 | K+、Na+、NH4+、Fe2+、Ba2+、Cu2+ |
| 阴离子 | OH-、I-、NO3-、AlO2-、HCO3-、HSO4- |
①A中的化学键类型为离子键、共价键(填“离子键”、“共价键”).
②A、B溶液混合后加热呈中性,该反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A的化学式为FeI2.
②经分析上述过程中溶液变黄的原因可能有两种(请用文字叙述)
Ⅰ仅有I-被氧化成I2使溶液呈黄色.ⅡI-、Fe2+均被氧化使溶液呈黄色.
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理(其他合理亦可).
④利用上述过程中溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为NO3-+4H++3e-═NO↑+2H2O.
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
| A. | 乳酸 CH3-CHOH-COOH | |
| B. | 甘油 CH2OH-CHOH-CH2OH | |
| C. | 脱氧核糖 CH2OH-CHOH-CHOH-CH2-CHO | |
| D. | 核糖 CH2OH-CHOH-CHOH-CHOH-CHO |


 .
.