题目内容
2.下列实验所采取的方法正确的是( )| A. | 除去甲酸乙酯中甲酸和乙醇,加入饱和纯碱溶液,振荡静置后分液 | |
| B. | 除去蛋白质溶液中氨基酸,加Na0H溶液后分液 | |
| C. | 分离高级脂肪酸钠和甘油,加水后分液 | |
| D. | 除去甲苯中的苯酚,加入过量浓溴水后过滤 |
分析 A.甲酸甲酯不溶于饱和纯碱,乙醇乙溶于水;
B.氨基酸与氢氧化钠反应生成氨基酸钠,反应后溶液不分层;
C.分离高级脂肪酸钠和甘油,应用盐析的方法;
D.三溴苯酚、溴都溶于甲苯中.
解答 解:A.甲酸甲酯不溶于饱和纯碱,乙醇乙溶于水,加入饱和纯碱溶液后溶液分层,可分液分离,故A正确;
B.氨基酸与氢氧化钠反应生成氨基酸钠,与蛋白质都溶于水,溶液不分层,不能用分液的方法分离,且蛋白质含有羧基,也与氢氧化钠反应,故B错误;
C.分离高级脂肪酸钠和甘油,应用盐析的方法,可加入饱和食盐水后分离,故C错误;
D.加入溴水,苯酚与溴水反应生成三溴苯酚,反应后三溴苯酚、溴都溶于甲苯中,不能得到纯净的甲苯,故D错误.
故选A.
点评 本题考查物质的分离、提纯,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同,除杂时注意不能引入新杂质,把握实验的严密性可行性的评价,难度不大.

练习册系列答案
相关题目
4.氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术.有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气.光伏发电是当今世界利用太阳能最主要方式之一.图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列说法不正确的是( )
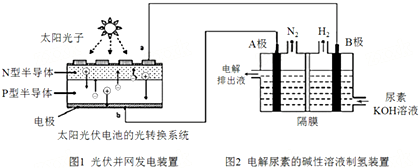

| A. | 图1中N型半导体为负极 | |
| B. | 若A极产生7.00gN2,则此时B极产生16.8L H2(标况下) | |
| C. | 电解完毕后电解液的pH增大 | |
| D. | 该系统工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O |
5.下列物质中属于混合物的是( )
①盐酸 ②液氯 ③漂白粉 ④碘酒 ⑤氯水.
①盐酸 ②液氯 ③漂白粉 ④碘酒 ⑤氯水.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②③④ |
10.甲烷、乙烯、苯都能发生的反应为( )
| A. | 加成反应 | B. | 聚合反应 | C. | 氧化反应 | D. | 水解反应 |
17.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示, 下列判断错误的是( )
下列判断错误的是( )
 下列判断错误的是( )
下列判断错误的是( )| A. | 三种酸的电离常数关系:KHA>KHB>KHD | |
| B. | 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| C. | pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |
14.下列分析中正确是( )
| A. | 含有碳元素的化合物不一定是烃 | |
| B. | 正丁烷分子中四个碳原子可能在同一直线上 | |
| C. | 常温常压下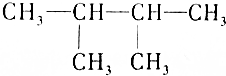 呈气态 呈气态 | |
| D. | 烷烃在任何情况下均不与强酸、强碱、氧化剂反应 |


 ;
; ,反应类型是取代反应;
,反应类型是取代反应;
 .
.