题目内容
1.把0.1mol MgCl2固体溶于水配成100mL溶液,此溶液中Cl-的物质的量浓度为( )| A. | 3.Omol•L-1 | B. | 2.Omol•L-1 | C. | O.3mol•L-1 | D. | O.2mol•L-1 |
分析 根据氯化镁的化学式计算出氯离子的物质的量,然后根据c=$\frac{n}{V}$计算出氯离子的物质的量浓度.
解答 解:0.1mol氯化镁中含有0.2mol氯离子,所得溶液中氯离子的物质的量浓度为:c=$\frac{0.2mol}{0.1L}$=2mol/L,
故选B.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的理念的概念及表达式为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
11.某由C、H、O元素组成的有机物球棍结构模型如图所示,下列说法中不正确的是( ) 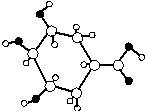

| A. | 该有机物不含苯环 | |
| B. | 分子式为C7H12O4 | |
| C. | 能与NaHCO3溶液反应生成CO2 | |
| D. | 1mol该有机物与足量的金属钠反应产生2molH2 |
12.下列实验操作正确的是( )
| A. | 用带橡皮塞的棕色细口瓶盛放浓硝酸 | |
| B. | 滴定管经蒸馏水润洗后,即可注入标准液进行滴定 | |
| C. | 用干燥清洁的玻璃棒蘸取某溶液点在pH试纸中部,跟标准比色卡比较来测定该溶液的pH | |
| D. | 配制溶液时加水超过容量瓶的标线,用滴管把多余的液体吸出 |
9.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2 L 0.5 mol/L硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| D. | 3mol单质Fe完全转变为Fe3O4失去8NA个电子 |
16.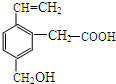 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )
①可以燃烧;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应;⑥能发生水解反应.
 某有机物的结构为如图所示,这种有机物可能具有的性质是( )
某有机物的结构为如图所示,这种有机物可能具有的性质是( )①可以燃烧;②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应;⑥能发生水解反应.
| A. | ①②④ | B. | ①②③④⑤ | C. | ①③④⑤⑥ | D. | ①②④⑥ |
10.有1L0.5mol/LNaOH溶液,取出0.2L后,以下对该溶液的叙述正确的是( )
| A. | 该溶液的体积变为0.8L | B. | 该溶液的物质的量浓度为0.5mol/L | ||
| C. | 该溶液的物质的量为0.5mol | D. | 该溶液的物质的量浓度为0.4mol/L |
11.下列关于氟氯烃的说法不正确的是( )
| A. | 氟氯烃是一类含氟和氯的卤代烃 | |
| B. | 氟氯烃的化学性质不稳定,有毒 | |
| C. | 氟氯烃大多数无色、无臭、无毒 | |
| D. | 在平流层,氟氯烃在紫外线照射下,分解产生的氯原子可引发损耗O3的循环反应 |
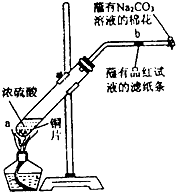 在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题:
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题: