题目内容
9.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 2 L 0.5 mol/L硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| D. | 3mol单质Fe完全转变为Fe3O4失去8NA个电子 |
分析 A、重水的摩尔质量为20g/mol;
B、溶液中的阴离子除了硫酸根外,还有氢氧根;
C、丙烯酸中含有碳碳双键和碳氧双键;
D、铁完全转化为四氧化三铁后变为+$\frac{8}{3}$.
解答 解:A、重水的摩尔质量为20g/mol,故18g重水的摩尔质量为0.9mol,则含9NA个质子,故A错误;
B、溶液中的阴离子除了硫酸根外,还有氢氧根,故溶液中含有的阴离子所带的电荷数大于NA个,故B错误;
C、丙烯酸中含有碳碳双键和碳氧双键,故0.1mol丙烯酸中含0.2NA个双键,故C错误;
D、铁完全转化为四氧化三铁后变为+$\frac{8}{3}$,0.3mol铁转变为四氧化三铁失去0.8mol电子即0.8NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
19.下列电子式书写正确的是( )
| A. | 氨气 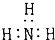 | B. | 四氯化碳  | C. | 氮气 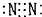 | D. | 过氧化氢 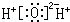 |
20.图1是碳的正常循环,但由于过度燃烧化石燃料,造成二氧化碳浓度不断上升.研究和解决二氧化碳捕集、存储和转化问题成为当前化学工作者的重要使命.
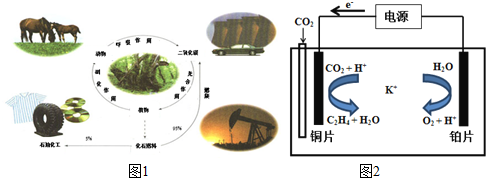
(1)有关碳循环的说法中正确的是ac
a.光合作用是光能转化成化学能
b.化石燃料是可再生的
c.循环过程有氧化还原反应
d.石油中含乙烯、丙烯,通过加聚反应得到高分子化合物
(2)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2发生反应:2CO2(g)═2CO(g)+O2(g),该反应的△H>0,(选填:>、<、=).
(3)CO2转化途径之一是:利用太阳能或生物质能分解水制H2,然后将H2与CO2转化为甲醇或其它的物质.
2H2O(1)═2H2(g)+O2(g)△H=+571.5kJ•mol-1
3H2(g)+CO2(g)═CH3OH(l)+H2O(1)△H=-137.8kJ•mol-1
则反应:4H2O (1)+2CO2(g)═2CH3OH(l)+3O2(g)△H=+1438.9kJ•mol-1.
你认为该方法需要解决的技术问题有:ab.
a.开发高效光催化剂
b.将光催化制取的氢气从反应体系中有效分离,并与CO2催化转化.
c.二氧化碳及水资源的来源供应
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体 NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见下表.( t1<t2<t3)
氨基甲酸铵分解反应是吸热 反应(“放热”、“吸热”).在15℃,此反应的化学平衡常数为:4×10-6.
(5)用一种钾盐水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图).在阴极上产生乙烯的电极反应方程式为:2CO2+12H++12e-=CH2=CH2+4H2O.

(1)有关碳循环的说法中正确的是ac
a.光合作用是光能转化成化学能
b.化石燃料是可再生的
c.循环过程有氧化还原反应
d.石油中含乙烯、丙烯,通过加聚反应得到高分子化合物
(2)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2发生反应:2CO2(g)═2CO(g)+O2(g),该反应的△H>0,(选填:>、<、=).
(3)CO2转化途径之一是:利用太阳能或生物质能分解水制H2,然后将H2与CO2转化为甲醇或其它的物质.
2H2O(1)═2H2(g)+O2(g)△H=+571.5kJ•mol-1
3H2(g)+CO2(g)═CH3OH(l)+H2O(1)△H=-137.8kJ•mol-1
则反应:4H2O (1)+2CO2(g)═2CH3OH(l)+3O2(g)△H=+1438.9kJ•mol-1.
你认为该方法需要解决的技术问题有:ab.
a.开发高效光催化剂
b.将光催化制取的氢气从反应体系中有效分离,并与CO2催化转化.
c.二氧化碳及水资源的来源供应
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体 NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见下表.( t1<t2<t3)
温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
(5)用一种钾盐水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图).在阴极上产生乙烯的电极反应方程式为:2CO2+12H++12e-=CH2=CH2+4H2O.
17.设阿伏加德罗常数的值为NA,下列叙述正确的是( )
| A. | 标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2NA | |
| B. | 0.1mol${\;}_{35}^{81}$Br原子中含中子数为3.5NA | |
| C. | 6.0g SiO2晶体中含有的硅氧键数目为0.4NA | |
| D. | 7.8g过氧化钠中所含有的阴离子数为0.2NA |
14.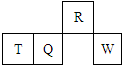 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | W对应的单质只可以跟强碱反应 |
1.把0.1mol MgCl2固体溶于水配成100mL溶液,此溶液中Cl-的物质的量浓度为( )
| A. | 3.Omol•L-1 | B. | 2.Omol•L-1 | C. | O.3mol•L-1 | D. | O.2mol•L-1 |
 .
.