题目内容
14.NA代表阿伏加德罗常数的值.下列叙述正确的是( )| A. | 标准状况下,11.2 L水中含有的氢氧键数为NA | |
| B. | 250 mL 1 mol•L-1FeCl3溶液中,阴、阳离子总数为NA | |
| C. | 一定条件下,将1mol SO2和0.5 mol O2充入一密闭容器内,充分反应后的生成物分子数为NA | |
| D. | 在反应2Na2O2+2CO2═2Na2CO3+O2中,每生成0.5 molO2转移的电子数为NA |
分析 A、标况下水为液态;
B、Fe3+是弱碱阳离子,在溶液中会水解;
C、二氧化硫和氧气的反应为可逆反应;
D、在反应2Na2O2+2CO2═2Na2CO3+O2中,氧元素的价态由-1价变为0价.
解答 解:A、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和含有的氧氢键的个数,故A错误;
B、Fe3+是弱碱阳离子,在溶液中会水解:Fe3++3H2O?Fe(OH)3+3OH-,导致阳离子个数增多,故溶液中的阴阳离子个数多于NA个,故B错误;
C、二氧化硫和氧气的反应为可逆反应,不能进行彻底,故生成的产物分子小于NA个,故C错误;
D、在反应2Na2O2+2CO2═2Na2CO3+O2中,氧元素的价态由-1价变为0价,故当生成0.5mol氧气时,转移NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
4.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,下列说法不正确的是( )
| A. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 | |
| B. | 淀粉和纤维素水解的最终产物都能发生银镜反应 | |
| C. | 实验时不小心将浓硝酸滴到皮肤上,皮肤表面会变黄 | |
| D. | 动物脂肪发生皂化反应,能生成甘油和高级脂肪酸钠 |
5.下列叙述中正确的是( )
| A. | 在稀溶液中,1mol酸和1mol碱完全反应所放出的热量叫做中和热 | |
| B. | 在101kPa时,1mol物质燃烧时的反应热叫做该物质的燃烧热 | |
| C. | 对于热化学方程式S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2,化学反应的△H前者大于后者 | |
| D. | 如果反应物所具有的总能量低于生成物所具有的总能量,则发生的反应是放热反应 |
9.在镁与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6mol/L,则10s内生成硫酸镁的平均反应速率是( )
| A. | 0.06 mol/(L•s) | B. | 1.8mol/(L•s) | C. | 1.2 mol/(L•s) | D. | 0.18 mol/(L•s) |
19.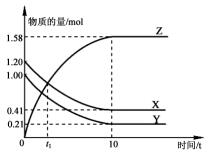 一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s) | |
| B. | t1时,Z和X的浓度相等,达到了化学平衡状态 | |
| C. | 反应开始到10 s时,Y的正逆反应速率都相等 | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |
6.下列化学方程式或离子方程式正确的是( )
| A. | 溴苯的制备: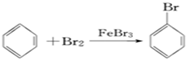 | |
| B. | 1,3-戊二烯发生加聚反应 | |
| C. | 苯酚钠溶液中通入少量二氧化碳: | |
| D. | 醇可以制备卤代烃,如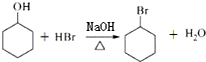 |
3.如图是常见四种有机物的比例模型示意图.下列说法正确的是( )
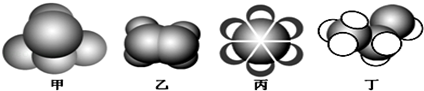

| A. | 甲能使酸性KMnO4溶液褪色 | |
| B. | 乙可与溴水发生加成反应而使溴水褪色 | |
| C. | 丙与浓硫酸、浓硝酸的混合液共热发生取代反应 | |
| D. | 丁可与NaHCO3发生取代反应 |
4.以极性键结合的多原子分子,分子是否有极性取决于分子的空间构型.下列分子都属于含极性键的非极性分子的是( )
| A. | CO2 H2O | B. | NH3 BCl3 | C. | P4 CH4 | D. | CS2 BF3 |
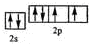 ,该元素的名称是氧;
,该元素的名称是氧;