题目内容
3.如图是常见四种有机物的比例模型示意图.下列说法正确的是( )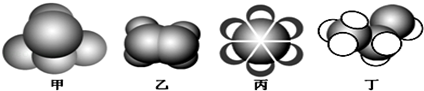
| A. | 甲能使酸性KMnO4溶液褪色 | |
| B. | 乙可与溴水发生加成反应而使溴水褪色 | |
| C. | 丙与浓硫酸、浓硝酸的混合液共热发生取代反应 | |
| D. | 丁可与NaHCO3发生取代反应 |
分析 A.由图可知,甲为甲烷,为饱和烃;
B.乙为乙烯,含碳碳双键;
C.丙为苯,苯环上H可发生取代反应;
D.丁为乙醇.
解答 解:A.由图可知,甲为甲烷,为饱和烃,与高锰酸钾不反应,故A错误;
B.乙为乙烯,含碳碳双键,可与溴水发生加成反应而使溴水褪色,故B正确;
C.丙为苯,与浓硫酸、浓硝酸的混合液共热发生取代反应生成硝基苯,故C正确;
D.丁为乙醇,与NaHCO3不反应,故D错误;
故选BC.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质及应用,题目难度不大.

练习册系列答案
相关题目
13.食品安全日益受到人们关注.下列食品能食用的是( )
| A. | 甲醛浸泡的海产品 | |
| B. | 霉变的大米、花生 | |
| C. | 用亚硝酸钠(NaNO2)代替食盐烹调的食品 | |
| D. | 食盐腌制的咸鸭蛋 |
14.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L水中含有的氢氧键数为NA | |
| B. | 250 mL 1 mol•L-1FeCl3溶液中,阴、阳离子总数为NA | |
| C. | 一定条件下,将1mol SO2和0.5 mol O2充入一密闭容器内,充分反应后的生成物分子数为NA | |
| D. | 在反应2Na2O2+2CO2═2Na2CO3+O2中,每生成0.5 molO2转移的电子数为NA |
11.下列各组顺序的排列正确的是( )
| A. | 单质氧化性:I2>Br2>Cl2 | B. | 热稳定性:PH3>H2S>HCl | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
18.已知:H2CO3 Ka1=4.3×10-7Ka2=5.61×10-11
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
| A. | 向碳酸氢镁溶液中加入足量的氢氧化钡溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液通入少量CO2的离子反应方程式:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 用惰性电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 向Ca(ClO)2溶液中通入少量CO2的离子反应方程式:Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓ |
8.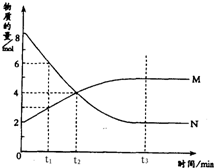 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A. | t1时,N的浓度是M浓度的2倍 | |
| B. | 反应的化学方程式为N?2M | |
| C. | t2时,正逆反应速率相等,达到平衡状态 | |
| D. | t3时,正反应速率小于逆反应速率 |
15.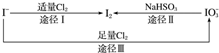 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示,下列说法中不正确的是( )| A. | 足量Cl2能使湿润的、已变蓝的淀粉KI试纸褪色的原因可能是5Cl2+I2+6H2O═2HIO3+10HCl | |
| B. | 途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA | |
| C. | 用淀粉KI试纸和食醋检验加碘盐时淀粉KI试纸会变蓝 | |
| D. | 由图可知氧化性的强弱顺序为Cl2>I2>IO${\;}_{3}^{-}$ |
12.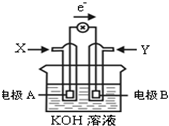 如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
 如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )
如图为某种甲醇燃料电池示意图,工作时电子流向如图所示.下列判断正确的是( )| A. | X为氧气 | |
| B. | 电极A反应式:CH3OH-6e-+H2O=CO2+6H+ | |
| C. | B电极附近溶液pH增大 | |
| D. | 电池工作时,溶液中电子由电极B流向电极A |