题目内容
1.有5种元素X、Y、Z、Q、T.X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满.下列叙述不正确的是( )| A. | 元素Y和Q可形成化合物Y2O3 | |
| B. | T和Z各有一种单质的空间构型为正四面体形 | |
| C. | X的最高价氧化物的立体构型为三角锥型 | |
| D. | ZO2是极性键构成的非极性分子,Z原子的杂化方式为sp杂化 |
分析 5种元素X、Y、Z、Q、T,X原子M层上有2个未成对电子且无空轨道,外围电子排布式为3s23p4,则X为S元素;Y原子的特征电子构型为3d64s2,则Y为Fe元素;Z原子的L电子层的p能级上有一个空轨道,外围电子排布式为2s22p2,则Z为C元素;Q原子的L电子层的P能级上只有一对成对电子,外围电子排布式为2s22p4,则Q是O元素;T原子的M电子层上p轨道半充满,外围电子排布式为3s23p3,则T是P元素.
解答 解:5种元素X、Y、Z、Q、T,X原子M层上有2个未成对电子且无空轨道,外围电子排布式为3s23p4,则X为S元素;Y原子的特征电子构型为3d64s2,则Y为Fe元素;Z原子的L电子层的p能级上有一个空轨道,外围电子排布式为2s22p2,则Z为C元素;Q原子的L电子层的P能级上只有一对成对电子,外围电子排布式为2s22p4,则Q是O元素;T原子的M电子层上p轨道半充满,外围电子排布式为3s23p3,则T是P元素.
A.Y是Fe元素、Q是O元素,二者形成的氧化物有氧化亚铁、氧化铁和四氧化三铁,所以元素Y和Q可形成化合物Fe2O3,故A正确;
B.T是P元素、Z是C元素,T和Z各有一种单质的空间构型为正四面体形,分别为白磷和金刚石,但白磷分子中四个磷原子位于四个顶点上,故B正确;
C.X是S元素,最高价氧化物为三氧化硫,三氧化硫中S原子没有孤对电子,价层电子对数为3,为平面三角形,故C错误;
D.ZO2是CO2,只含极性键,为直线形对称结构,为非极性分子,碳原子为sp杂化,故D正确.
故选C.
点评 本题考查原子结构和元素周期律,侧重考查学生分析判断能力,关键是根据核外电子排布推断元素,熟练掌握元素化合物知识,掌握空间结构、杂化方式、分子极性判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.2,3-二甲基丁烷可生成多少种不同沸点的一溴代物( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
12.某元素一种同位素的原子的质子数为m,中子数为n,则下列说法正确的是( )
| A. | 这种元素的原子量为m | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | (m+n)可写在该元素符号的左上角 | |
| D. | 核内中子的总质量小于质子的总质量 |
16.现有核电荷数小于20的元素A,其电离能数据如下:(I1表示失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:×102 kJ•mol-1)
(1)外层电子离核越远,能量越高,电离能越小(填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越大(填“大”或“小”).
(2)上述11个电子分属3个电子层.
(3)失去了11个电子后,该元素还有1个电子.
(4)该元素最高价氧化物对应水化物的化学式是Mg(OH)2.
| 序号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电力能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 序号 | I7 | I8 | I9 | I10 | I11 | … |
| 电力能 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
(2)上述11个电子分属3个电子层.
(3)失去了11个电子后,该元素还有1个电子.
(4)该元素最高价氧化物对应水化物的化学式是Mg(OH)2.
13.一定量的某饱和一元醛发生银镜反应,析出银21.6g,等量的此醛完全燃烧时生成CO2 8.96L(标况),则此醛是( )
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 2-甲基丁醛 |
10.某混合气体由两种气态烃组成,取2.24L该混合气体完全燃烧得到4.48L二氧化碳(气体体积已折算为标准状况)和3.6g水,则这两种气体可能是( )
| A. | CH4和C3H8 | B. | CH4和C3H4 | C. | C2H4和C2H6 | D. | C2H2和C2H6 |
11.键线式可以简明扼要地表示碳氢化合物,键线式为 的物质是( )
的物质是( )
 的物质是( )
的物质是( )| A. | 丙烷 | B. | 丁烷 | C. | 丙烯 | D. | 丁烯 |
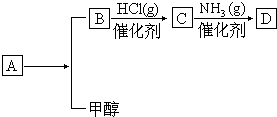
 、
、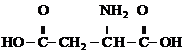 .
.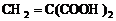 .
.