题目内容
4.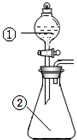 用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硫酸 | 用砂纸打磨过的铝条 | 无明显现象 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 稀硝酸 | 铜片 | 立即产生大量红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀盐酸先和NaOH反应生成NaCl,然后和碳酸钠反应生成NaHCO3,最后NaHCO3再和HCl反应生成CO2;
B.浓硫酸和Al发生钝化现象;
C.将氯化铝加入NaOH溶液中先生成NaAlO2;
D.Cu和稀硝酸反应生成无色NO,NO不稳定,易被空气氧化生成红棕色气体NO2.
解答 解:A.稀盐酸先和NaOH反应生成NaCl,然后和碳酸钠反应生成NaHCO3,最后NaHCO3再和HCl反应生成CO2,所以不能立即产生气体,则结论不正确,故A错误;
B.浓硫酸和Al发生氧化还原反应而生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以没有明显现象,故B正确;
C.将氯化铝加入NaOH溶液中先生成可溶性的NaAlO2,则先没有明显现象,当氯化铝过量时二者反应生成白色沉淀,所以结论不正确,故C错误;
D.Cu和稀硝酸反应生成无色NO,NO不稳定,易被空气氧化生成红棕色气体NO2,所以结论不正确,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质之间的反应、物质的性质,明确实验原理、物质性质是解本题关键,注意C中滴加顺序不同导致产物不同、反应现象不同,为易错点.

练习册系列答案
相关题目
5.由碳原子构成的纳米碳管可以作为储存氢气的优良容器,其单层部分结构示意图如图,下列说法正确的是( )

| A. | 纳米碳管是一种无机化合物 | |
| B. | 0.12g纳米碳管中含有6.02×l022个碳原子 | |
| C. | 纳米碳管与石墨互为同位素 | |
| D. | 纳米碳管中碳原子间以共价键结合 |
15.标准状况下,将NO2、NO、O2 混合并充满容器,然后把容器倒置于水槽中,充分反应后,水充满容器,则容器中HNO3溶液的物质的量的浓度(mol/L)用M表示范围是( )
| A. | $\frac{1}{28}$<M<$\frac{1}{22.4}$ | B. | $\frac{1}{39.2}$<M<$\frac{1}{22.4}$ | C. | $\frac{1}{39.2}$<M<$\frac{1}{28}$ | D. | 0<M<$\frac{1}{22.4}$ |
12.某元素一种同位素的原子的质子数为m,中子数为n,则下列说法正确的是( )
| A. | 这种元素的原子量为m | |
| B. | 不能由此确定该元素的相对原子质量 | |
| C. | (m+n)可写在该元素符号的左上角 | |
| D. | 核内中子的总质量小于质子的总质量 |
19.下列各表述与示意图一致的是( )
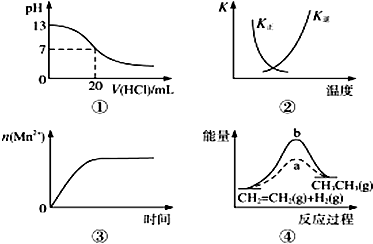

| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的p随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol•L-1 KMnO4酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. | 图④中a、b曲线分别表示反应CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化 |
16.现有核电荷数小于20的元素A,其电离能数据如下:(I1表示失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:×102 kJ•mol-1)
(1)外层电子离核越远,能量越高,电离能越小(填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越大(填“大”或“小”).
(2)上述11个电子分属3个电子层.
(3)失去了11个电子后,该元素还有1个电子.
(4)该元素最高价氧化物对应水化物的化学式是Mg(OH)2.
| 序号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电力能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 序号 | I7 | I8 | I9 | I10 | I11 | … |
| 电力能 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
(2)上述11个电子分属3个电子层.
(3)失去了11个电子后,该元素还有1个电子.
(4)该元素最高价氧化物对应水化物的化学式是Mg(OH)2.
13.一定量的某饱和一元醛发生银镜反应,析出银21.6g,等量的此醛完全燃烧时生成CO2 8.96L(标况),则此醛是( )
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 2-甲基丁醛 |
14.NA代表阿伏加罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,60gCH3COOH中含共用电子对数为7NA | |
| B. | 56g聚乙烯含有的碳原子数为4NA | |
| C. | 2molSO2和1molO2在密闭容器中充分反应后,容器内物质分子数等于2NA | |
| D. | 2L0.5mol/L乙酸溶液中H原子数为0.1NA |
 、
、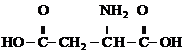 .
.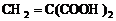 .
.