题目内容
3.下列关于甲苯的性质描述中,能说明侧链对苯环有影响的是( )| A. | 甲苯与氢气可以发生加成反应 | B. | 甲苯燃烧带有浓厚的黑烟 | ||
| C. | 甲苯能使酸性高锰酸钾溶液褪色 | D. | 甲苯硝化生成三硝基甲苯 |
分析 侧链对苯环有影响,使苯环变得活泼,更容易发生取代反应,所以甲苯硝化时能生成三硝基甲苯.
解答 解:A、甲苯和氢气发生加成反应是由苯环的结构特点决定的,与侧链对苯环的影响无关,故A错误;
B、甲烷和甲苯都能燃烧产生带浓烟的火焰,这是碳不完全燃烧导致,所以不能说明侧链对苯环有影响,故B错误;
C、甲苯能使高锰酸钾溶液褪色的原因是甲苯中的甲基被高锰酸钾溶液氧化,体现了苯环对侧链的影响,故C错误;
D、甲苯和苯都能与浓硝酸、浓硫酸发生取代反应,但产物不同,侧链对苯环有影响,使苯环变得活泼,更容易发生取代反应,甲苯硝化生成三硝基甲苯,能说明侧链对苯环有影响,故D正确.
故选D.
点评 本题以侧链对苯环的影响为载体考查了苯的同系物的化学性质,难度不大,注意:苯环对甲基的影响导致甲苯能被酸性高锰酸钾氧化成甲酸,而同时苯环对侧链也有影响甲苯能使酸性高锰酸钾褪色.

练习册系列答案
相关题目
9.电子表中电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,放电时锌极上的电极反应是:Zn+2OH--2e-═Zn(OH)2;氧化银电极上的反应式为:Ag2O+H2O+2e-═Ag+2OH-,总反应式为:Ag2O+H2O+Zn═Zn(OH)2+2Ag.下列说法正确的是( )
| A. | 锌是阴极,氧化银是阳极 | |
| B. | 锌发生还原反应,氧化银发生氧化反应 | |
| C. | 溶液中OH-向Ag2O极移动,K+、H+向Zn极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液的pH基本保持不变 |
14.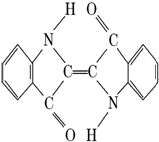 历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )
历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )
 历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )
历史上最早应用的还原性染料是靛蓝,其结构简式如右图,下列关于靛蓝的叙述中错误的是( )| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 该物质属于芳香化合物 | D. | 它含有碳碳双键和酯基 |
8.下列各组物质中,分子中的所有原子都满足最外层8电子结构的是( )
①BeCl2、PF5 ②PCl3、N2 ③COCl2(光气)、SF6 ④XeF2、BF3 ⑤SO2、H2O2、HClO.
①BeCl2、PF5 ②PCl3、N2 ③COCl2(光气)、SF6 ④XeF2、BF3 ⑤SO2、H2O2、HClO.
| A. | ①② | B. | ③④ | C. | ② | D. | ⑤ |
15.用NA表示阿伏伽德罗常数的值.下列叙述中不正确的是( )
| A. | 标准状况下,22.4 L一氯甲烷中有5 NA个原子 | |
| B. | 17.6 g丙烷中含有3.2 NA个极性共价键 | |
| C. | 13 g苯和苯乙烯的混合液体中有2 NA个原子 | |
| D. | 分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
13.室温下,用0.1g金属粉末与10mL酸溶液反应,在反应开始阶段,产生H2的速率最快的是( )
| 金属(粉末状) | 酸的浓度 | |
| A | Mg | 6 mol/L硝酸 |
| B | Zn | 3 mol/L硫酸 |
| C | Fe | 6 mol/L盐酸 |
| D | Cu | 6 mol/L硫酸 |
| A. | A | B. | B | C. | C | D. | D |
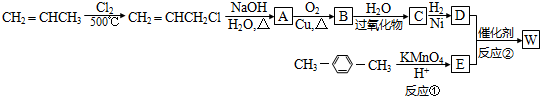
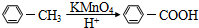
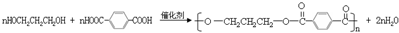 .
.