题目内容
18.以下有7种物质:①铜 ②稀硫酸③氯化氢、氯化铁溶液 ④液氨 ⑤H2S ⑥二氧化碳 ⑦石灰水,把序号填入下列各空中:(1)强电解质的是:③
(2)电解质在熔融状态下并不导电③⑤
(3)在水溶液中部分电离的电解质⑤.
(4)既不是电解质,也不是非电解质,但能导电①②⑦.
分析 (1)电解质是在水溶液或熔化状态下能导电的化合物,能全部电离的电解质是强电解质;
(2)电解质是在水溶液或熔化状态下能导电的化合物,金属氧化物、碱、盐在熔融状态下能导电,酸、弱碱只在水溶液中电离而能导电;
(3)电解质是在水溶液或熔化状态下能导电的化合物,在水溶液中部分电离的电解质属于弱电解质;
(4)金属单质能导电,溶液能导电,但单质、混合物都既不是电解质,也不是非电解质.
解答 解:(1)氯化氢在水溶液里能全部电离,所以都是强电解质,故答案为:③;
(2)氯化氢、H2S水溶液中电离而导电,在熔化状态下不导电,且属于电解质,故答案为:③⑤;
(3)H2S是一种二元弱酸,是在水溶液中部分电离的电解质,故答案为:⑤;
(4)铜属于金属单质,能导电,稀硫酸、石灰水溶液能导电,但属于混合物,则它们既不是电解质,也不是非电解质,但能导电,故答案为:①②⑦..
点评 本题较简单,考查物质的分类、电解质、非电解质的概念及导电的原因,明确概念的要点及常见物质的组成或构成即可解答.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
4.有A、B、C、D四种金属,将A与B用导线连结起来,浸入电解质溶液中,A易腐蚀.将A、D分别投入等物质的量浓度盐酸中,D比A反应剧烈.将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出.据此判断它们的活动性由强到弱的顺序是( )
| A. | D>A>B>C | B. | A>D>B>C | C. | D>A>C>B | D. | C>B>A>D |
6.下列各分子中所有原子都满足最外层为8电子稳定结构的是( )
| A. | H2O | B. | CH4 | C. | BF3 | D. | PCl3 |
3.下列关于甲苯的性质描述中,能说明侧链对苯环有影响的是( )
| A. | 甲苯与氢气可以发生加成反应 | B. | 甲苯燃烧带有浓厚的黑烟 | ||
| C. | 甲苯能使酸性高锰酸钾溶液褪色 | D. | 甲苯硝化生成三硝基甲苯 |
7.相同温度、相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g)?3W(g)+2Z(g)△H=-Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表,下列说法正确的是( )
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出a kJ/mol | ||
| 乙 | 1mol | 1mol | 放出b kJ/mol | ||
| 丙 | 2mol | 2mol | 放出c kJ/mol | ||
| 丁 | 3mol | 2mol | 吸收d kJ/mol |
| A. | 平衡时丙容器中Z的物质的量浓度最大 | |
| B. | c+d<Q | |
| C. | 平衡时,甲容器中的反应速率比丁容器中的慢 | |
| D. | X的转化率为:甲<乙<丙 |
8.下列有关氯元素的说法中,正确的是( )
| A. | 最高正化合价为+7 | B. | Cl2中含有极性共价键 | ||
| C. | HClO4比H2SO4酸性弱 | D. | Cl是卤素中原子半径最小的 |
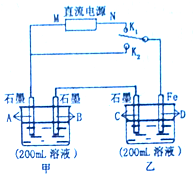 如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)
如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)