题目内容
8.下列各组物质中,分子中的所有原子都满足最外层8电子结构的是( )①BeCl2、PF5 ②PCl3、N2 ③COCl2(光气)、SF6 ④XeF2、BF3 ⑤SO2、H2O2、HClO.
| A. | ①② | B. | ③④ | C. | ② | D. | ⑤ |
分析 对于共价化合物,元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,据此进行判断.
解答 解:①中Be是4号元素,不可能达8电子;P为ⅤA族且为最高价,不是8电子,故①错误;
②P是“5+|-3|=8”,Cl是“7+|-1|=8”,N2中存在氮氮三键,N原子最外层满足8电子稳定结构,所以PCl3、N2都满足8电子结构,故②正确;
③中SF6的S为+6价,不是8电子,故③错误;
④中稀有气体Xe在化合物中比8电子多,BF3中B不是8电子,故④错误;
⑤中SO2的S为+4价,不是8电子,H2O2和HClO中的H也不是8电子,故⑤错误;
故选C.
点评 本题考查原子的结构,题目难度不大,注意熟练掌握判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
相关题目
19.下列关于铜电极的叙述中不正确的是( )
| A. | 铜锌原电池中铜是正极 | |
| B. | 铁壳船底部镶嵌铜块,铜块更易被腐蚀 | |
| C. | 用电解法精炼粗铜时粗铜作阳极 | |
| D. | 在镀件上镀铜是可用金属铜作阳极 |
3.下列关于甲苯的性质描述中,能说明侧链对苯环有影响的是( )
| A. | 甲苯与氢气可以发生加成反应 | B. | 甲苯燃烧带有浓厚的黑烟 | ||
| C. | 甲苯能使酸性高锰酸钾溶液褪色 | D. | 甲苯硝化生成三硝基甲苯 |
13.下列说法不正确的( )
| A. | 互为同分异构体的物质化学性质不一定相似 | |
| B. | 等物质的量的烃A和烃B完全燃烧时,消耗相等物质的量的氧气,则A和B的相对分子质量的差值可能为16 | |
| C. | 如果烃中各元素的质量百分含量都相同,则它们必定是同分异构体 | |
| D. | 氰酸铵(NH4OCN)与尿素[CO(NH2)2]互为同分异构体 |
20.对于碳及其化合物间转化的说法中,正确的是( )
| A. | 大气中CO2含量的剧增,对自然界中碳及其化合物间的平衡没有影响 | |
| B. | 木炭燃烧过程中,存在碳单质、CO和CO2之间的转化 | |
| C. | 碳的氧化物间的相互转化不属于氧化还原反应 | |
| D. | 含碳的无机化合物和有机化合物之间存在着严格的界限,无机化合物不能合成有机化合物 |
17.关于化工生产原理的叙述中,不符合目前工业生产实际的是( )
| A. | 硫酸工业中,三氧化硫在吸收塔内被水吸收制成浓硫酸 | |
| B. | 炼铁工业中,用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 | |
| C. | 合成氨工业中,用铁触媒作催化剂,可提高单位时间氨的产量 | |
| D. | 氯碱工业中,电解槽的阴极区产生NaOH |
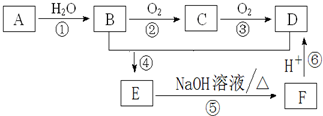 已知:烃 A的摩尔质量为28g/mol,有关A的转化关系如图所示,请回答下列问题:
已知:烃 A的摩尔质量为28g/mol,有关A的转化关系如图所示,请回答下列问题: