题目内容
12.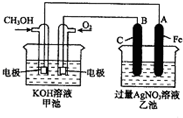 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O(1)请回答图中甲、乙两池的名称.甲电池是原电池装置,乙池是电解池装置.
(2)请回答下列电极的名称:通入CH3OH的电极名称是负极,B(石墨)电极的名称是阳极.
(3)写出电极反应式:通入O2的电极的电极反应式是O2+2H2O+4e-=4OH-.A(Fe)电极的电极反应式为4Ag++4e-=4Ag,
(4)乙池中反应的化学方程式为4AgNO4+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3.
分析 (1)根据方程式及燃料电池的特点判断甲装置;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极B是阳极;
(3)氧气在正极上得电子,铁为阴极,发生还原反应;
(4)乙池电解硝酸银生成银、硝酸和氧气.
解答 解:(1)根据反应方程式知,甲装置是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池,
故答案为:原电池;电解池;
(2)根据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,反应式为:CH3OH-6e-+8OH-=CO32-+6H2O;O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极B是阳极;故答案为:负极;阳极;
(3)据2CH3OH+3O2+4KOH=2K2CO3+6H2O知,CH3OH发生氧化反应,所以该电极是负极,O2 得电子和水反应生成氢氧根离子,发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极是阳极该电极上发生氧化反应,电极反应为:O2+2H2O+4e-=4OH-,
Fe极为阴极,发生还原反应生成银,电极方程式为 4Ag++4e-=4Ag,
故答案为:O2+2H2O+4e-=4OH-; 4Ag++4e-=4Ag;
(4)乙池电解硝酸银生成银、硝酸和氧气,电解方程式为4AgNO4+2H2O $\frac{\underline{\;通电\;}}{\;}$ 4Ag+O2↑+4HNO3,故答案为:4AgNO4+2H2O $\frac{\underline{\;通电\;}}{\;}$ 4Ag+O2↑+4HNO3.
点评 本题考查了原电池和电解池的工作原理的应用,侧重于学生的分析能力的考查,题目涉及电池判断、电极判断,电解方程式的书写、电子守恒的应用等,题目难度中等.

 |  |  |  |
| A.接近称量质量时,轻振手腕,加够药品 | B.溶解时,用量筒控制所加蒸馏水的量 | C.移液时,玻璃棒插在刻度线以上,防止液体洒出 | D.接近刻度线1~2 cm时,用胶头滴管滴加蒸馏水至刻度线 |
| A. | A | B. | B | C. | C | D. | D |
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下生成甲醇蒸气和水蒸气.图表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图.
①能判断该反应向正反应方向进行的是:B
A.v正(H2)=3v逆(CH3OH)

B.容器中混合气体的密度变大
C.容器中压强不变
D.2个C=O断裂的同时有6个H-H形成
②上述反应其他条件保持不变,在恒容条件下进行,平衡时H2的转化率将变小(填“变大”“变小”或“不变”)
③写出上述反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49kJ•mol-1
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)═CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量mol | 平衡量mol | 达平衡所需时间min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值:$\frac{1}{6}$(填具体值或取值范围)
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为2mol,则此时v正<v逆(填“<”“>”或“=”)
(3)甲醇在一定条件下能转化为甲醛,碘量滴定法是测定甲醛的化学方法之一,其原理是在碱性介质(NaOH)中,碘转化为次碘酸钠和碘化钠,后将溶液中游离的甲醛氧化为甲酸钠,经适当酸化后,剩余的次碘酸钠和碘化钠又生成碘,上述过程中甲醛参与的化学反应的离子方程式为:HCHO+IO-+OH-=HCOO-+I-+H2O.
| A. | 溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤 | |
| B. | 转移溶液前容量瓶内有少量蒸馏水 | |
| C. | 定容时,俯视容量瓶的刻度线 | |
| D. | 定容摇匀时,发现液面降低,又补加少量水,重新达到刻度线 |
| A. | pH=3的HNO 3与pH=11的KOH溶液 | |
| B. | pH=3的HNO 3与pH=11的氨水 | |
| C. | pH=3的H 2SO 4与pH=11的NaOH溶液 | |
| D. | pH=3的CH 3COOH与pH=11的Ba(OH) 2溶液 |

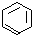 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质编号),HCHO分子的立体构型为平面三角形.